���嵥Ԫ �������仯���1.1��
2015-11-09 11:10:19 ��Դ�� �壺��Х ��Ӱ���� ; ���ۣ�0 �����
���嵥Ԫ �������仯���1.1��
|
|
|
�ڿ��ˣ��� Х |
|
|
���˽��Ƶ�ԭ�ӽṹ���������ʣ����淽���� |
|
|
��ѧĿ�꣺ |
�������ơ������ơ��������Ƶ���Ҫ���ʡ� |
|
|
|
������̼���ơ�̼�����Ƶ����ʡ�ת�����Ʒ���
|
|
|
��ѧ�ص㣺 |
��������������ʺͻ�ѧ���ʡ���������ʵIJ��켰�ݱ���� |
|
|
��ѧ�ѵ㣺 |
Na2O2��Na2CO3��NaHCO3���������ƶ�����ʽ���� |
|
|
��ѧ������ |
���ݺ�������Ų����ö�λ���Ʋ⻯ѧ���ʣ�Ȼ����ȥ������ |
|
|
��ѧ���̣� |
��һ��ʱ |
|
����֪ʶ����
һ���ƺ��ƵĻ�����
�Ƽ��仯����֮���ת����ϵ��

1����
��1���Ƶ��������ʣ�
��������ɫ�Ĺ��壬�������ܶȱ�ˮС��0.97 g��cm3�����۵�Ϊ97.81�������Ⱥ͵�������塣
��2���ƵĻ�ѧ���ʣ�
��ԭ��������Ӳ���ֻ��һ�����ӣ��ڷ�Ӧ�м���ʧȥ1�����ӣ����ֽ�ǿ�Ļ�ԭ�ԡ�
Na![]()
![]()
����ǽ������ʵķ�Ӧ��
2Na+O2![]() Na2O2 (����ʻ�ɫ)
Na2O2 (����ʻ�ɫ)
4Na+O2=2Na2O (����ɫ�䰵)
2Na+S=Na2S
����ˮ��Ӧ��
2Na+2H2O=2NaOH+H2�� (�������Ρ��ۡ��졢��)
�� NaH+H2O=NaOH+H2��
![]() ����˼��
����˼��![]()
1�����ձ��м���ˮ�ͱ�(�����ܶ�Ϊ0.88 g��cm��3����ˮ�������ܣ��Ҳ����Ʒ�Ӧ)��50 mL����һС��������(�ܶ�Ϊ0.97 g��cm��3)Ͷ���ձ��У��۲쵽�����������ʲô��
2���Ʒֱ���ˮ���ᷴӦʱ����һ��������Щ������ϡ�ᷴӦʱ������H2O��Ӧ����������������H����Ӧ��
3����һС����Ͷ�뵽CuSO4��Һ�У��ɹ۲쵽��������ʲô����д����صĻ�ѧ����ʽ��
�����εķ�Ӧ
a����������̬�η�Ӧ���ƿɽ������õĽ����û�������������4Na+TiCl4=4NaCl+Ti.
b����������Һ��Ӧʱ����������ˮ��Ӧ����NaOH���ٿ�������NaOH��Ӧ����Ӧ�����û�����Һ�еĽ�����
I����������ͭ��Һ��Ӧ��2Na+2H2O+CuSO4=Cu(OH)2��+Na2SO4+H2��
II�����뱥��ʳ��ˮ��Ӧ:2Na��2H2O=2NaOH+H2��(�ų����壬��������)
III�������Ȼ����Һ��Ӧ:2Na+2NH4Cl=2NaCl+2NH3��+ H2��
IV������̼��������Һ��Ӧ:2Na+2NaHCO3=2Na2CO3 +H2��
V���������Ȼ�����Һ��Ӧ:4Na+AlCl3+2H2O=NaAlO2+3NaCl+2H2��
VI�������Ȼ�������Һ��Ӧ:
8Na+4FeCl2+O2+10H2O =4Fe(OH)3��+8NaCl+4H2��
���ܷ���ʽ��д�����Ƚ�������Ӧ�Ļ�ѧ����ʽд����Ȼ���ٽ�������Ӧ�е��м�������������õ��ܷ���ʽ���ܷ���ʽ�ڽ��ijЩ���ӵĻ�ѧ��Ӧ�����У����ŷdz���Ҫ�����塣
�����ڿ����еı仯��
���仯���̣�
Na��Na2O(����Na2O2)��NaOH��Na2CO3��Na2CO3��10H2O��Na2CO3�����յõ���ɫ��ĩ��
���Ƶı��棺����ú���У�����������
(3)���屣�棺����Ӧ�����ڹ��ƿ�У��������������еijɷַ�Ӧ����Ӧ�ܷⱣ�棬�����ر���õ����ʻ�ӦҺ�⡣�ڲ�ȡҺ��ʱ��Ӧ���ǹ������Һ���Ƿ�Ӧ���ܽ⣬�ܶȴ�С��Һ���Ƿ�ӷ������ء�
(4) �Ƶ���;
����ȡNa2O2�Ȼ����
���ơ��غϽ�(Һ̬)������ԭ�ӷ�Ӧ�ѵĵ��ȼ���
���������Դ��������ѹ�Ƶơ�
��ұ��ijЩ������
�����ƾ���ǿ�Ļ�ԭ�ԣ�����״̬�¿���������ȡ��������4Na��TiCl44NaCl��Ti��
˵������ҵ����850 ������������״̬��KCl��Ӧ������ȡ�����أ�Na(l)��KCl(l)NaCl(l)��K(g)����Ӧ��������Ϊ�ڷ�Ӧ�¶��£���ϵ��ֻ�м������壬�ܴ���ϵ���ݳ������ڷ�Ӧ������У����ڷ�Ӧ�¶��£�Ϊ������Ӧ���÷�Ӧ����˵�������ƵĻ�ԭ��ǿ�ڽ����أ�
��˼ά��ģ��
����һ����������H2O�������ᷴӦ��ʵ��
1����һС������Ʒֱ�Ͷ��ʢaˮ��b�Ҵ���cϡH2SO4������С�ձ��У���Ӧ�����ɿ쵽����˳��Ϊ_______�����ͷ�Ӧ���ʲ�ͬ��ԭ��__________��
����c>a>b�����������������ʷ�Ӧ��ʵ�ʶ�������H������û���Ӧ��H��Ũ�ȵĴ�С�����˷�Ӧ���ʵĿ��������������ʵ���H����������֪H��Ũ�ȵĴ�С˳��Ϊc>a>b�������Ӧ����Ϊc>a>b��
�������������������Һ������Һ��Ӧ��ʵ��
2���������Ʒ���ʢ��������Һ��С�ձ��У��������壬���а�ɫ������������_______��
��MgSO4��Һ����NaCl��Һ����Na2SO4��Һ�������ͳ���ʯ��ˮ����Ca(HCO3)2��Һ����CuSO4��Һ��������NaCl��Һ
�����٢ܢݢ�
������2Na��2H2O===2NaOH��H2��������Mg2����2OH��===Mg(OH)2�������з�Ӧ����ˮ����Һ�¶����ߣ�Ca(OH)2���ܽ�Ƚ��ͣ�����Ca(OH)2��������������Ca2����HCO��OH��===CaCO3����H2O�������ɵ�Cu(OH)2����ɫ���������������⣻��ˮ���٣�c(Na��)����ʹNaCl(s)���Na��(aq)��Cl��(aq)ƽ�������ƶ���
3��������� ��һ���ڸ�������������������FeSO4��Һ��Ӧ�ķ�������֤��Ӧʵ�ʡ�ʵ��ʱ����100 mL���Թ����ȼ�40 mLú�ͣ�ȡ3��������С�Ľ����Ʒ�����Թܺ�������Ƥ����ͨ������©������FeSO4��Һʹú�͵�Һ�������������н����ɼ�(��ͼ)����ϸ�۲죬�ش��������⣺
��һ���ڸ�������������������FeSO4��Һ��Ӧ�ķ�������֤��Ӧʵ�ʡ�ʵ��ʱ����100 mL���Թ����ȼ�40 mLú�ͣ�ȡ3��������С�Ľ����Ʒ�����Թܺ�������Ƥ����ͨ������©������FeSO4��Һʹú�͵�Һ�������������н����ɼ�(��ͼ)����ϸ�۲죬�ش��������⣺
(1)��δ��Լ�ƿ��ȡ�ý����ƣ�ʣ���Na�ܷ�Ż�ԭ�Լ�ƿ��
(2)�й��Ʒ�Ӧ��������_______________________��
(3)���Թܵ���Һ�г��ֵ�����________________________��
(4)װ����Һ��ı仯�����Թ���________������©����____________��
(5)д����������������Һ��Ӧ�Ļ�ѧ����ʽ��_________��
����(1)�����Ӵ��Լ�ƿ��ȡһ������ƣ�����ֽ���ɱ����ϵ�ú�ͣ���С���ڲ���Ƭ����������С������ʵ���ã�ʣ�����Ҫ�Ż�ԭ�Լ�ƿ����Ҫ���ⶪ����
(2)���������ɣ����ۻ���С������ú�ͺ�FeSO4��Һ���洦����������������ȫ�ܽ�
(3)�²���Һ���ְ�ɫ��״����
(4)�½�������
(5)2Na��FeSO4��2H2O===Fe(OH)2����Na2SO4��H2��
2�������ƺ������ƣ�
(1)��ѧʽ�� Na2O�� Na2O2
(2)���ʣ�
Na2O�ǰ�ɫ���壬Na2O2�ǵ���ɫ���壨��ɫ�����ڻ�ѧ�в�����������ƶ����п��ܻ�������Ӧ����ע�⣩��
Na2O���ڼ�����������м����������ͨ�ԣ�Na2O2�����ڼ�����������Ƕ�����H2O��CO2��HCl�ȷ�Ӧ��
2Na2O2+2H2O��4NaOH+O2�� Na2O+H2O=2NaOH
2Na2O2+2CO2=Na2CO3+O2�� Na2O+CO2=Na2CO3
2Na2O2+4HCl=4NaCl+2H2O+O2�� Na2O+2HCl=2NaCl+H2O
ע����
��Na2O2����ǿ������������������������������Ư����ɱ������Na2O2����ʹƷ����Һ��ɫ��ʹʯ����Һ�ȱ�������ɫ��
��������CO2��H2O�ĵ�һ���ʻ��Ƕ��ߵĻ���ͨ��������Na2O2ʱ��CO2��H2O��ų�O2�����ʵ���֮�Ⱦ�Ϊ2��1��
����CO2��ˮ�����Ļ������(��һ����)ͨ������Na2O2����������ļ���������ԭ��������������Ҳ������������������
����Na2O2��CO2��H2O��Ӧʱ�����ʵ�����ϵΪ2Na2O2��O2��2e����
��һ������Na2O2��һ������CO2��H2O(g)�Ļ����ķ�Ӧ��������Na2O2����CO2��Ӧ����CO2��Ӧ��ȫ��Na2O2����H2O������Ӧ��
�������뼼�ɡ�Na2O2��CO2��H2O��Ӧʱ���൱�ڹ���(Na2O2)ֻ������CO2�е���CO����H2O�е���H2�������Կ���������Ӧ�ķ�Ӧ��Na2O2��CONa2CO3��Na2O2��H22NaOH(ʵ��������Ӧ�����ܷ���)��
��������ɷ���(CO)m��(H2)n�����ʣ�W g ��������O2����ȫȼ�գ��������(CO2��ˮ����)ͨ��������Na2O2�������ر�ΪW g��������C��H��O����Ԫ����ɵ����ʣ�ֻҪC��Oԭ�Ӹ�����Ϊ1��1�����������������
��ѧ�γ����ķ�����һ��ϵ�������У�
a�����H2��CO��H2��CO�Ļ�����壻
b���л��CH3OH(�״�)��HCHO(��ȩ)��CH3COOH(����)��HCOOCH3(�������)��C6H12O6(������)�ȡ�
��˼���뽻����
1��Na2O2�У����������Ӹ������Ƕ��٣����Ǽ�����������
2�������ʵ�����Na2O��Na2O2�ֱ�Ͷ�������������ˮ�У�������Һ�����ʵ���Ũ����ʲô��ϵ��������Һ���������Ƿ���ȣ�
3�����ס��ҡ��������ĸ��ձ��ڷֱ����0.1 mol���ơ������ơ��������ƺ��������ƣ�Ȼ�������100 mL ��ˮ�����裬ʹ������ȫ�ܽ⡣��ס��ҡ���������Һ�����ʵ�����������С��˳����(����)
A����<��<��<�� B����<��<�ң���
C���ף���<�ң��� D����<��<��<��
4��(1)д��CO2��Na2O2��Ӧ�Ļ�ѧ����ʽ��______________________��
(2)ijѧ���ж�SO2��Na2O2��Ӧ�����������ƣ�����Ϊ�����жϺ����𣿼�Ҫ˵�����ɣ� _________________________________��
(3)��ͬѧ���϶���Ӧ���Ƿ����������ɣ���ʹ����ͼ��ʾװ�ý���ʵ��(ͼ������̨��װ������ȥ)��
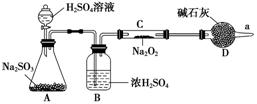
װ����B��������__________________________��
D��������_____________________________________________��
(4)Ϊȷ�Ϸ�Ӧ�����ͬѧ���������ʵ�鲽�裬����ΪӦ���еIJ�����˳��������(ѡ�����)________��
A���ô����ǵ�ϸľ����������ܿ�a���۲�ϸľ���Ƿ��Ż�ȼ��
B����Cװ���з�Ӧ��Ĺ���������������ˮ�����Һ
C������ɵ���Һ�м����������ữ�����ᱵ��Һ���۲��Ƿ��г�������
D������ɵ���Һ���ȼ������ᣬ�ټ����Ȼ�����Һ���۲��Ƿ������ݻ��������
����(1)2CO2��2Na2O2===2Na2CO3��O2 ��(2)���������ڹ������ƾ���ǿ�����ԣ��ܽ���4�۵�������Ϊ��6�۵�������������ơ�
(3)����SO2���壬��ֹˮ��������Cװ����Na2O2��Ӧ����ֹ�����е�ˮ��������Cװ����Na2O2��Ӧ����������ͬʱ���չ���SO2���壬���������ļ���ͷ�ֹ��Ⱦ������
(4)ABD
5����10��ƽ����Է�������Ϊ20��CO�� H2 �Ļ�����壬��96�� O2 ��Ϻ��ֵ�ȼ��Ȼ�������ͨ��234��Na2O2�У���Ӧ������������������������ٿˣ������壺234��10=244g�����壺96g��
��˼ά��ģ��
����һ���������Ƶ�ǿ������
1���Ƚ��������鷴Ӧ���ش��������⡣
һ�飺��Na2O2��CO2��������Na2O2��SO2
���飺��Na2O2��FeCl3(��Һ) ��Na2O2��FeCl2(��Һ)
���飺��SO2ͨ��Ʒ����Һ�У����ȡ���Na2O2���뵽Ʒ����Һ�У�����
���飺��NaOH��Һ������ɫʯ����Һ�С���Na2O2������뵽��ɫʯ����Һ��
���⣺(1)д������������Ӧ�Ļ�ѧ����ʽ��
(2)�ж���������Ӧ�п��ܷ���������Ϊʲô��
(3)�ж���������Ӧ�п��ܷ���������Ϊʲô��
(4)�ж���������Ӧ�п��ܷ���������
����(1)��2Na2O2��2CO2===2Na2CO3��O2 ��Na2O2��SO2===Na2SO4
(2)��������Ӧ�����к��ɫ�������ɲ�������ų�����������������������������FeCl3��NaOH��Ӧ����Fe(OH)3��Fe(OH)3�Dz����Եĺ��ɫ����������Fe2������ǿ��ԭ�����ױ�Na2O2����������Fe(OH)3��Na2O2����Һ�е�ˮ���ҷ�Ӧ����O2������
(3)����Һ��ɫ��ȥ�����Ⱥ��ָֻ���ɫ������Һ��ɫ��ȥ�����Ⱥ��ָܻ���ɫ��ԭ����SO2��Ư���Բ��ȶ���Na2O2��Ư�������������ǿ�����ԡ�
(4)����Һ����������Һ�ȱ�������ɫ��ԭ����Na2O2��H2O��Ӧ����NaOH���ʼ��ԣ�ͬʱNa2O2����Ư���ԡ�
2��ij��Һ�к���HCO��SO��CO��CH3COO��4�������ӡ������м���������Na2O2�������Һ������Ũ�Ȼ������ֲ������(������Һ����ޱ仯) (����)
A��CH3COO�� B��SO C��CO D��HCO
����A
������Na2O2��ˮ��Ӧ����NaOH��HCO��OH��===CO��H2O��HCOŨ�ȼ�С��COŨ������SO���л�ԭ�ԣ���Na2O2������Ũ�ȼ�С��CH3COO���������䡣
��������й�Na2O2�Ķ�������
3�����ס��ҡ��������ĸ��ձ��ڷֱ����0.1 mol���ơ������ơ��������ƺ��������ƣ�Ȼ�������100 mLˮ�����裬ʹ������ȫ�ܽ⣬��ס��ҡ���������Һ�����ʵ�����������С˳���� (����)
A���ף��ң������� B�������ף��ң���
C���ף������ң��� D�������ף��ң���
����B
������(1)�ס�����ȣ�
�ף�Na��NaOH��������H2O���ܼ����٣�����NaOH��Ӧ�����ܼ�����
��NaOH��������������>����
(2)�ҡ�����ȣ�
NaOH�������H2O����ܼ����
���ҡ�����Һ��ȫ��ͬ��
(3)�ҡ��������� �ף�Na�����ң�Na2O��������Na2O2
���������ʵ������ʱ��Na(��)����NaOH���ҡ���(Na2O��Na2O2)����NaOH���ʵ����������������ĵ�ˮ��ȣ����ܼ���ȣ���˼������������ҡ���С��
4�����ʵ�����ͬ��N2��O2��CO2��Ϻ�ͨ��Na2O2����һ��ʱ�䣬��������Ϊԭ������������(ͬ��ͬѹ��)����ʱN2��O2��CO2�����ʵ���֮��Ϊ (����)
A��1��1��0 B��6��9��0 C��3��4��1 D��3��3��2
����C
�������跴ӦǰN2��O2��CO2�������Ϊ3����Ӧǰ�����Ϊ9����Ӧ�������Ϊ8��
2Na2O2��2CO2===2Na2CO3��O2��������V
2 1 1
2 1 (9��8)��1
����Ӧ����CO2 2���������O2 1������ʷ�Ӧ����V(N2)��3��V(O2)��3��1��4 ��V(CO2)��3��2��1�����ߵ�����ȼ�Ϊ���ʵ���֮����Ϊ3��4��1��
5��ȡa gij������O2����ȫȼ������������������Na2O2������ȫ��Ӧ����Ӧ��������ǡ��Ҳ������a g���������ʲ������������������ (����)
A��H2 B��CO C��C6H12O6 D��C12H22O11
����D
������2CO��O22CO2 ��
2Na2O2��2CO2===2Na2CO3��O2 ��
����������Na2O2��CO===Na2CO3(����ķ�Ӧ)����CO�ɱ�Na2O2��ȫ����
2H2��O22H2O ��
2Na2O2��2H2O===4NaOH��O2�� ��
����������Na2O2��H2===2NaOH(����ķ�Ӧ)
C��ɱ���Ϊ(CO)6(H2)6��D���ΪC��(CO)11(H2)11�������Ӧ���������Ӵ���a g��
6��1 mol����������2 mol̼�����ƹ����Ϻ������ܱ������м��ȳ�ַ�Ӧ���ų��������ʺ���ȴ�������Ĺ��������� (����)
A��Na2CO3 B��Na2O2�� Na2CO3
C��NaOH ��Na2CO3 D��Na2O2 ��NaOH�� Na2CO3
�𰸣�A
������̼�����ƹ������ȷ����ֽⷴӦ��2NaHCO3Na2CO3��CO2����H2O�������ɵ�CO2��H2O������Na2O2��Ӧ��2CO2��2Na2O2===2Na2CO3��O2��2H2O(g)��2Na2O2===4NaOH��O2�����ݼ�����ϵ��֪��2 mol̼���������ȷֽ�����CO2��H2O(g)��1 mol��Na2O2ֻ��1 mol������ǡ�ú�CO2��Ӧ����Na2CO3��O2[Ҫע��Na2O2��CO2��H2O(g)�ķ�Ӧ�Ⱥ�˳��]���ų��������ʺ���ֻʣ��Na2CO3��
�����������������������ʶ����Ե�ʵ��̽��
7��ij�о���ѧϰС���Na2O2���й�����̽�����£�����з�̪��ˮ��Ͷ��һ������Na2O2���۲쵽���д������ݲ�������Һ��죬��һ�����Һ�ֱ�Ϊ��ɫ��������ʵ������Һ��죬��һ�������ɫ��ԭ�ס�����ͬѧ����˲�ͬ�Ľ��ͣ�
��ͬѧ��Ϊ��Na2O2��ˮ��Ӧ�ų������������������ԣ�����̪������ʹ��Һ��ɫ����ͬѧ����Ϊ��Na2O2��ˮ��Ӧʱ������H2O2��H2O2��ǿ������ʹ��̪��ɫ��
(1)��ͬѧ���������ʵ����֤���Լ��IJ�������ȷ�ģ��ڵ��з�̪������������Һ�еμ�3%��H2O2��Һ����
������ͬѧ�IJ�����ȷ���ɹ۲쵽��������_______________��
����ͬѧ�����ͬѧ��������֤ʵ�������Ӧ����ʵ����ܸ�ֱ��֤��Na2O2��ˮ��Ӧ������H2O2����ͬѧ���Ҫ���ӵ�ʵ����ʲô��
(2)����Ƽ�ʵ��֤����ͬѧ�Ľ����Ƿ���ȷ(��������װ��ͼ��˵����Ҫ����)��
����(1)����Һ�ĺ�ɫ��ȥ
���ڵ��з�̪��ˮ�м��������������ƣ�����Ӧ��ɺ�����Һ�м��������������̷�ĩ��������ų���֤������������ˮ��Ӧʱ��H2O2���ɡ�
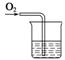 (2)����з�̪������������Һ��ͨ������������ɫ��ȥ��֤����ͬѧ���Ʋ���ȷ����֮������ȷ��ʵ��װ��ͼ��ͼ��ʾ(���ù��ƿ���������������ձ�����������)
(2)����з�̪������������Һ��ͨ������������ɫ��ȥ��֤����ͬѧ���Ʋ���ȷ����֮������ȷ��ʵ��װ��ͼ��ͼ��ʾ(���ù��ƿ���������������ձ�����������)
������(1)����Һ�ĺ�ɫ��ȥ������ΪH2O2��Ư���ԣ���Ư��̪����H2O2��MnO2�����ܷų����������ڼ���������ƺ��ˮ��Һ�м�������MnO2�������ݷų���ֱ��֤������������ˮ��Ӧ��H2O2���ɡ�
(2)���Ҫ��֤������������̪���������з�̪������������Һ��ֱ��ͨ�����������顣
8��(1)�ں�����ߺ�DZˮͧ�п��ù���������Ϊ����������ѡ���ʵ��Ļ�ѧ�Լ���ʵ����Ʒ������ͼ�е�ʵ��װ�ý������飬֤���������ƿ�����������
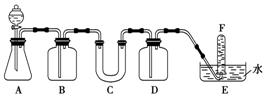
��A����ȡCO2��װ�á�д��A�з�����Ӧ�Ļ�ѧ����ʽ��__________��
��B��ʢ����NaHCO3��Һ����������__________________��
��д�����������������̼��Ӧ�Ļ�ѧ����ʽ_________________��
��D��ʢ�ŵ��Լ���____________����Ŀ����_____________��
���Թ�F���ռ����������һ��ʵ�������__________________��
(2)��ijѧ���ж�SO2��Na2O2��Ӧ�����������ƣ�����Ϊ�����жϺ�����__________����Ҫ˵�����ɣ� ___________________________��
����ͬѧ���϶���Ӧ���Ƿ����������ɣ���ʹ����ͼ��ʾװ�ý���ʵ��(ͼ������̨��װ������ȥ)��
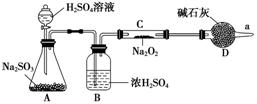
װ����B��������___________________��D��������__________________��
��Ϊȷ�Ϸ�Ӧ�����ͬѧ���������ʵ�鲽�裬����ΪӦ���еIJ�����˳��������________(ѡ�����)��
A���ô����ǵ�ϸľ����������ܿ�a���۲�ϸľ���Ƿ��Ż�ȼ��
B����Cװ���з�Ӧ��Ĺ���������������ˮ�����Һ
C������ɵ���Һ�м����������ữ�����ᱵ��Һ���۲��Ƿ��г�������
D������ɵ���Һ���ȼ������ᣬ�ټ����Ȼ�����Һ���۲��Ƿ������ݻ��������
����(1)��CaCO3��2HCl===CaCl2��CO2����H2O������ȥCO2�����е�HCl����2Na2O2��2CO2===2Na2CO3��O2����NaOH��Һ������δ��Ӧ��CO2������E�еĵ����Ƴ�ˮ�棬�رշ�Һ©����������Ĵָ��ס�Թܿڣ�ȡ���Թܣ������Ѵ����ǵ�ľ�������Թܿ��ڣ�ľ����ȼ��֤���Թ����ռ���������������
(2)�����������ڹ������ƾ���ǿ�����ԣ��ܽ���4�۵�������Ϊ��6�۵�������������ơ�
������SO2���壬��ֹˮ��������Cװ����Na2O2��Ӧ��ֹ�����е�ˮ������CO2����Cװ����Na2O2��Ӧ����������ͬʱ���չ���SO2���壬���������ļ���ͷ�ֹ��Ⱦ������
��ABD
���̺�ǡ�
��һƪ����5��Ԫ ������Ҫ��ѧ��Ӧ�ܽ�.ppt
��һƪ�����嵥Ԫ �������仯���1.2��
