第十三单元 化学实验(2)
2015-12-01 08:31:36 来源: 撰稿:董啸 摄影摄像: ; 评论:0 点击:
第十三单元 化学实验(2)
|
|
|
授课人:董 啸 |
|
|
①了解一般事故处理方法,能对常见物质进行检验、分离和提纯。
|
|
|
教学目标: |
②了解实验室常用仪器的主要用途和用法,能根据要求配制溶液。
|
|
|
|
③掌握化学实验的基本操作,掌握常见气体的实验室制法。 |
|
|
教学重点: |
物质的制备、检验、分离提纯 |
|
|
教学难点: |
设计、评价或改进实验方案 |
|
|
教学方法: |
分析比较法 |
|
|
教学过程: |
第二课时 |
|
基础知识精析
2、化学实验基本操作
(1)物质的溶解
①气体物质溶解时,根据溶解度的不同采用不同的方法.溶解度较小的气体(如:Cl2、H2S、SO2、CO2等)导气管直插水中;极易溶解于水的气体(如HCI.NH3等)应将导气管靠近液面或导管口连一个倒扣的漏斗,并使漏斗边缘刚好贴靠液面。

②液体物质溶解时用量筒分别量取一定体积被溶解的液体和溶剂,然后先后加入烧杯中搅拌而溶解。若溶解放热较多的液体,应将密度大的液体注入密度小的液体中,边加边搅拌(如稀硫酸的配制应将浓H2SO4倒入水中)。
③固体物质一般在试管或烧杯中进行,块状固体先要研细,后加水搅拌,振荡或加热等措施。
(2)物质的加热
①加热的方式:加热的方式可分为直火加热、垫石棉网加热、水浴加热、油浴(或砂浴)加热几种。
②加热温度和受热容器选择:试管、坩埚、蒸发皿、燃烧匙可用灯焰直接加热,而烧杯、烧瓶等仪器要垫石棉网加热。加热时,受热容器外壁不能有水,要防止容器受热不均而破裂。
对某些温度不超过100摄氏度的实验(如银镜反应、实验室制硝基苯和测定溶解度等),则要求用水浴来加热,这是为了使受热均匀且便于控制反应的温度。
③给试管里的固体加热,应将管口略微向下倾斜,以防形成的水滴倒流至管底而引起试管破裂。操作时,先要将试管均匀受热再将火焰固定加热盛有固体的试管底部。
④对盛有液体的试管加热,要使管口向斜上方倾斜(约45。角),试管口不能对着人。加热时,还要不断振荡试管,以防止局部受热沸腾而飞溅。
(3)气密性检验
凡是有导气的实验装置,装配好后均需要检查气密性,且在放入药品之前检查。
①原理:使装置形成一个密闭体系,改变装置内气体的温度或体积,再使体系内气体产生压强变化,并产生某种明显的现象(气泡或液面变化),根据表现出来的某种现象去判断。
②常用方法:双手(或热毛巾)捂住容器使气体热膨胀,通过观察气泡的产生现象来判断装置的气密性。若要检查整套装置的气密性,为形成一定的气压差,产生明显的现象,可用酒精灯对装置中某个可加热的容器微热,观察插入液体的导管口是否有气泡冒出,从而判断整套装置的气密性是否良好。
装置气密性的检查方法
|
方法 |
微热法 |
液差法 |
外压法 |
|||||
|
原理 |
升高装置中气体的温度,使气体膨胀 |
缩小装置中气体的体积,增大压强 |
增大或减小装置中气体的物质的量 |
|||||
|
|
图例 |
|
|
|
|
|||
|
|
具体 操作 |
塞紧橡胶塞,将导气管末端伸入盛水的烧杯中,用手捂热(或用酒精灯微热)烧瓶 |
塞紧橡胶塞,用止水夹夹住导气管的橡胶管部分,从长颈漏斗向试管中注水 |
塞紧橡胶塞,打开止水夹推动或拉动注射器 |
|
|||
|
|
现象 说明 |
烧杯中有气泡产生,停止微热,冷却后导气管末端形成一段水柱,且保持一段时间不下降 |
停止加水后,长颈漏斗中的液面高于试管中的液面,且液面差不再改变 |
推动注射器之后导管中出现一段液柱,且液面差不改变,拉动注射器试管中产生气泡 |
|
|||
1.对下列装置,不添加其他仪器无法检查气密性的是 ( )

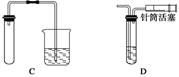
答案 A
解析 B项利用液差法:夹紧弹簧夹,从长颈漏斗中向试管内加水,长颈漏斗中会形成一段液柱,停止加水后,通过液柱是否变化即可检查;C项利用加热(手捂)法:用酒精灯加热(或用手捂热)试管,通过观察烧杯中有无气泡以及导管中水柱是否变化即可检查;D项利用抽气法:向外轻轻拉动注射器的活塞,通过观察浸没在水中的玻璃导管口是否有气泡冒出即可检查。
2.以下是实验室制取气体的三套常见装置:
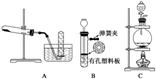
(1)装置A、B在加入反应物前,怎样检查其气密性?
(2)某同学准备用装置C制取SO2,并将制取的SO2依次通入品红溶液、澄清石灰水、酸性KMnO4溶液的试剂瓶,一次完成SO2的性质实验。上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法来证明该装置不漏气。
答案 (1)对装置A:将导管的出口浸入水槽的水中,手握住试管,有气泡从导管口逸出,放开手后,有少量水进入导管,且水柱保持一段时间不变,说明装置不漏气;对装置B:塞紧橡胶塞,夹紧弹簧夹后,从长颈漏斗注入一定量的水,使长颈漏斗内的水面高于试管内的水面,停止加水后,长颈漏斗中与试管中液面差保持不变,说明装置不漏气。
(2)反应前点燃酒精灯,加热烧瓶一小会儿。在盛放品红溶液、澄清石灰水、酸性KMnO4溶液的试剂瓶中出现气泡,停止加热后,浸没在溶液中的导管中上升一段水柱,且水柱保持一段时间不变,证明该装置不漏气。
解析 (1)对装置A,可使试管受热造成体积膨胀而观察;对装置B,一般通过在关闭弹簧夹后加液形成一段液柱进行观察确定。
(2)装置C后由于有不少连续装置,空间较大,用手掌紧贴烧瓶外壁产生的微弱热量不足以产生明显现象,此时可通过提高温度(微热)的方法检查装置气密性。
(4)试纸的使用
①常见试纸:石蕊试纸、pH试纸、品红试纸、KI淀粉试纸等。
——定性检验酸碱性
——定量(粗测)检测酸碱性强弱
——检验SO2等有漂白性的物质
——检验Cl2等有氧化性的物质
②使用方法:
检验液体:取一小块试纸放在表面皿或玻璃片上用玻璃棒沾取待测液点在试纸中部,观察试纸颜色的变化;
检验气体:用蒸馏水把试纸润湿粘在玻璃棒的一端,并使其接近试管口,观察颜色变化(注意:pH试纸使用时不能湿润)。
(5)仪器的洗涤
①洗涤干净的标志:仪器内壁附着的水均匀,既不成水滴,也不成股流下。
②洗涤步骤:先用自来水冲、再用洗涤液(根据附着的物质选择)洗、然后用自来水冲、最后蒸馏水润洗。
(6)药品的取用
①固体药品的取用
取用固体药品一般用药匙。往试管里装入固体粉末时,为避免药品沾在管口和管壁上,先使试管倾斜,把盛有药品的药匙(或用小纸条折叠成的纸槽)小心地送入试管底部,然后使试管直立起来,让药品全部落到底部。有些块状的药品可用镊子夹取。

②液体药品的取用
取用很少量液体时可用胶头滴管吸取。取用较多量液体时可用直接倾注法:取用细口瓶里的药液时,先拿下瓶塞,倒放在桌上,然后拿起瓶子(标签应对着手心)瓶、口要紧挨着试管口,使液体缓缓地倒入试管。注意防止残留在瓶口的药液流下来,腐蚀标签。一般往大口容器或容量瓶、漏斗里倾注液体时,应用玻璃棒引流。
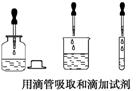
![]() 思考
思考![]() 取用药品时,应遵循节约的原则。多余的药品一般不能放回原瓶,但有些药品要放回原瓶。请问哪些药品要放回原瓶,为什么?
取用药品时,应遵循节约的原则。多余的药品一般不能放回原瓶,但有些药品要放回原瓶。请问哪些药品要放回原瓶,为什么?
答案 K、Na、白磷等,因随意丢弃易引起火灾等安全事故。
3、试剂使用和存放
(1)试剂使用:
实验室里所用的药品,很多是易燃、易爆、有腐蚀性或有毒的。因此,在使用时一定要严格遵照有关规定和操作规程,保证安全。
不能用手接触药品,不要把鼻孔凑到容器口去闻药品(特别是气体)的气味,不得尝任何药品的味道。注意节约药品,严格按照实验规定的用量取用药品。实验剩余的药品既不能放回原瓶,也不要随意丢弃,更不要拿出实验室,要放人指定的容器内。
(2)存放要求:
试剂存放时,应避免变质和泄露。保存时,易挥发或遇空气反应的应密封保存,受热或见光易分解的避光冷藏;固体试剂用广口瓶,液体试剂用细口瓶;瓶塞应与试液不反应。
(3)常见试剂保存方法:
常见试剂保存:钠、钾、白磷、硝酸、浓硫酸、氨水、盐酸、硝酸银、酒精、浓溴水、新制的氯水、苯酚、氢氧化亚铁、碱石灰、氢氧化钠、氢氟酸。
①钾、钙、钠在空气中极易氧化,遇水发生剧烈反应,应放在盛有煤油的广口瓶中以隔绝空气。
②白磷着火点低(40℃),在空气中能缓慢氧化而自燃,通常保存在冷水中。
③液溴有毒且易挥发,需盛放在磨口的细口瓶里,并加些水(水覆盖在液溴上面),起水封作用。
④碘易升华且具有强烈刺激性气味,盛放在磨口的广口瓶里。
⑤浓硝酸、硝酸银等见光易分解,保存在棕色瓶中,贮放在黑暗而且温度低的地方。
⑥氢氧化钠固体易潮解,应盛放在易于密封的干燥大口瓶中保存;其溶液盛放在无色细口瓶里,瓶口用橡皮塞塞紧,不能用玻璃塞。长时间存放不能使用玻璃瓶。
![]() 深度思考
深度思考![]()
1.取用药品时,应遵循节约的原则。多余的药品一般不能放回原瓶,但有些药品要放回原瓶。请问哪些药品要放回原瓶,为什么?
答案 K、Na、白磷等,因随意丢弃易引起火灾等安全事故。
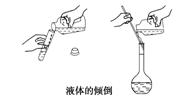
2.指出下图操作中的错误。

(1)取用金属颗粒_____________。(2)取大量液体______________。
(3)取少量液体__________________。
答案:(1)块状固体直接落入试管底部,易砸破试管;(2)①瓶塞正放在桌面上;②试剂瓶标签未面向手心;③试剂瓶瓶口未紧靠试管口;④试管未倾斜45°;(3)滴管伸入试管内
3.用pH试纸定量测定溶液的pH时,能用蒸馏水润湿吗?若润湿,一定会产生误差吗?
答案:不能。若润湿,不一定有误差,如测NaCl溶液的pH时。
![]()
1.下列实验基本操作错误的是 ( )
A.滴定管洗净后经所要盛装的液体润洗,即可注入标准液进行滴定
B.玻璃导管蘸水后,边旋转边向橡胶管中插入
C.将0.1 mol·L-1的NaOH溶液与0.5 mol·L-1的CuSO4溶液等体积混合制得氢氧化铜悬浊液,用于检验醛基
D.玻璃棒蘸取溶液滴到放在表面皿上的pH试纸上
答案 C
解析 A项是中和滴定实验的基本操作,滴定管必须用所要盛装的液体润洗后才能进行实验;B项是对有关仪器的连接知识的考查,玻璃导管和橡胶管的连接是仪器连接中最基本的连接;C项考查氢氧化铜悬浊液的配制,配制时要保证氢氧化钠过量;D项中有关pH试纸的使用也是要求学生掌握的一项基本操作。
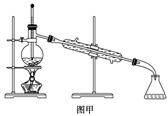
2.下列有关实验的叙述正确的是 ( )
A.可用碱式滴定管量取12.85 mL KMnO4溶液
B.实验室蒸馏石油可用如图甲所示实验装置
C.取用金属钠或钾时,没用完的钠或钾要放回原瓶
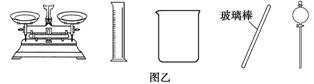
D.配制500 mL 0.4 mol·L-1 NaCl溶液,必要的仪器如图乙所示
答案 C
解析 解本题先要了解仪器的结构,在头脑中形成仪器的图像,记忆其主要用途和使用时的注意事项。A中KMnO4溶液具有强氧化性,不能用碱式滴定管量取;B中温度计的水银球应位于蒸馏烧瓶支管口处;D中不需要分液漏斗,而需要500 mL的容量瓶。
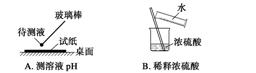
3.下列有关实验操作正确或能达到预期目的的是 ( )
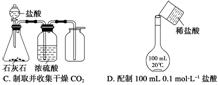
答案 C
解析 A错,试纸不能直接放在桌面上;B错,不能将水加到浓硫酸中,应将密度大的溶液加到密度小的溶液中;C中制备的CO2的密度大于空气的,可用向上排空气法收集,也能用浓硫酸干燥;D错,没有沿玻璃棒转移稀盐酸。
【教后记】
相关热词搜索:
上一篇:第十三单元 化学实验(1)
下一篇:第十三单元 化学实验(3)