第十三单元 化学实验(1)
2015-12-01 08:30:47 来源: 撰稿:董啸 摄影摄像: ; 评论:0 点击:
第十三单元 化学实验(1)
|
|
|
授课人:董 啸 |
|
|
①了解一般事故处理方法,能对常见物质进行检验、分离和提纯。
|
|
|
教学目标: |
②了解实验室常用仪器的主要用途和用法,能根据要求配制溶液。
|
|
|
|
③掌握化学实验的基本操作,掌握常见气体的实验室制法。 |
|
|
教学重点: |
物质的制备、检验、分离提纯 |
|
|
教学难点: |
设计、评价或改进实验方案 |
|
|
教学方法: |
分析比较法 |
|
|
教学过程: |
第一课时 |
|
基础知识精析
一、 仪器使用及实验室安全
1、化学实验常用仪器
(1)常见的加热仪器:①酒精灯 ②试管 ③烧杯 ④烧瓶 ⑤蒸发皿 ⑥蒸馏烧瓶 ⑦坩埚
直接加热的仪器:
①试管
a.给液体加热时液体的体积不超过试管容积的。
b.加热固体时试管口应略向下倾斜。
②蒸发皿:蒸发浓缩溶液时要用玻璃棒搅拌,液体体积不超过容积的。
③坩埚:用于灼烧固体,移动、使用时要用坩埚钳夹取。
(2)间接(垫石棉网)加热的仪器
①烧杯:溶解固体时需用玻璃棒搅拌,加热液体时,液体体积不超过容积的。
②圆底烧瓶:使用时液体的体积为烧瓶容积的~。
③锥形瓶:a.滴定时液体不超过容积的。
(2)用于物质分离的仪器
|
仪器 |
主要用途 |
使用方法和注意事项 |
|
普通漏斗 |
(1)向小口容器中转移液体 (2)加滤纸后,可过滤液体 |
(1)制作过滤器时,滤纸紧贴漏斗内壁,用水润湿,注意不得留有气泡 (2)滤纸上缘低于漏斗边缘,液体低于滤纸边缘 |
|
分液漏斗 |
(1)用于随时添加液体 (2)萃取、分液 |
(1)注意活塞不得渗漏 (2)分离液体时,下层液体由下口放出,上层液体由上口倒出 |
|
蒸发皿 |
蒸发或浓缩溶液 |
可直接加热,加热液体不超过其容积的2/3,快蒸干时停止加热 |
|
蒸馏烧瓶 |
蒸馏或分馏 |
(1)加热时要垫石棉网 (2)加热时液体的量不超过其容积的1/2 |
|
洗气瓶 |
除去气体中的杂质,其中广口瓶可换作大试管或锥形瓶 |
(1)一般选择与杂质气体反应的试剂作吸收剂 (2)装入液体量不宜超过容积的2/3 (3)气体的流向为A进B出 |
|
干燥管 |
用于干燥或吸收某些气体,干燥剂为粒状,常用CaCl2、碱石灰 |
(1)注意干燥剂或吸收剂的选择 (2)一般为大口进气,小口出气 |
(3) 常用的用于称量的仪器
①天平 ②量筒 ③滴定管(酸式滴定管和碱式滴定管) ④移液管
【学生活动】完成下列空白

(1)仪器A的名称:量筒,用途:量取一定体积的液体,精确度:0.1_mL。
特别提醒 (1)无“0”刻度;(2)不可加热,不可作反应容器,不可用于溶液的稀释;(3)选取量筒的规则是“大而近”,例如量取5.6 mL NaOH溶液应选取10 mL量筒,而不能选50 mL量筒。
(2)仪器B的名称:容量瓶,用途:配制一定物质的量浓度的溶液,该仪器能长时间贮存溶液吗?不能。
(3)仪器C的名称:酸式滴定管。
①使用前需“查漏”;②“0”刻度在上方;③用于盛装酸性溶液或强氧化性液体(如KMnO4溶液),不可盛装碱性溶液;④精确度:0.01 mL。
(4)仪器D的名称:碱式滴定管。
用于盛装碱性溶液,不可盛装酸性和强氧化性液体(如KMnO4溶液)。
(5)仪器E的名称:托盘天平。
①称量前先调零点;②腐蚀性药品应放于烧杯内称量;③左盘放被称物,右盘放砝码,即左物右码;④精确度:0.1 g。
(6)仪器F的名称:温度计。
①测反应混合物的温度时:应将温度计插入混合物中,温度计的水银球不能接触容器内壁,如测定物质的溶解度、实验室中制乙烯及中和热的测定;②测蒸气的温度时,水银球应在液面以上;测馏分温度时,水银球应略低于蒸馏烧瓶支管口处。
![]() 深度思考
深度思考![]()
1.上述常用仪器中使用前必须检查是否漏水的有哪些?
答案:必须检查是否漏水的有分液漏斗、容量瓶、酸式滴定管和碱式滴定管。
2.用干燥管作干燥器干燥H2时应选择何种干燥剂?
答案:应选碱石灰、CaO或NaOH固体等。
3.如图所示,读数时同样是仰视,引起的读数误差相同吗?

答案 不同,A图读数偏大,B图读数偏小。
(4)用于夹持支撑的仪器
①镊子:用于取块状固体;②试管夹:用于夹持试管(离管口1/3处);③坩埚钳:用于夹持坩埚;④铁架台(铁夹、铁圈)用于固定反应容器;⑤三角架(泥三角)。
(5)除杂常用的仪器
①洗气瓶 ②干燥管 ③U型管
(6)其它仪器
①玻璃棒:用于搅拌、引流、转移固体;②药匙:用于取粉状固体;③胶头滴管:用于滴加液体;④研钵:用于研细固体颗粒;⑤温度计:用于测量温度;⑥干燥管:用于干燥气体;⑦广口瓶:用于收集气体;⑧干燥器:用于盛放,加热后冷却易吸收水蒸气的物质(如胆矾中结晶水含量的测定实验中无水硫酸铜的冷却);⑨其它:玻璃管、橡皮塞、表面皿。
![]()
1.有如图所示A、B、C、D四种仪器:

请选择下列仪器名称的序号,填入相应的横线上:
①烧杯 ②碱式滴定管 ③圆底烧瓶 ④锥形瓶 ⑤分液漏斗 ⑥酸式滴定管。A:________B:________C:________D:________。
答案 ③ ⑤ ④ ⑥
2.下列仪器中,在灼烧固体物质时必须用到的仪器是________。(填名称)
![]()
答案 坩埚、泥三角
题组二 常用仪器使用注意事项
3.下列有关仪器用途的说法中正确的是 ( )
A.试管、烧杯均可用于给液体、固体加热
B.使食盐水中NaCl结晶析出时,常用到的仪器有坩埚、酒精灯、玻璃棒、泥三角
C.区别NaCl、Na2SO4时常用到胶头滴管、试管
D.漏斗可用于过滤及向滴定管中添加溶液
答案 C
解析 烧杯只能用于给液体加热,A错;使食盐水中NaCl晶体析出的方法通常是蒸发浓缩、冷却结晶,使用的仪器应是蒸发皿而不是坩埚,B错;由于物质鉴别所用试剂量较少,故应使用试管作反应容器,通过胶头滴管滴加试剂,C对;向滴定管中添加溶液的方法是直接将试剂瓶中的液体转移到滴定管中,D错。
4.下列操作中仪器使用不正确的是 ( )
A.用碱式滴定管盛装高锰酸钾溶液
B.用铁坩埚灼烧烧碱
C.用铁坩埚除去纯碱晶体中的结晶水
D.加热蒸发皿时不用石棉网
答案 A
解析 高锰酸钾溶液具有强氧化性能腐蚀碱式滴定管下端的橡胶管。
5.某学生的实验报告中有如下数据:①用托盘天平称取11.7 g食盐;②用量筒量取21.48 mL盐酸;③用容量瓶配制210 mL 1 mol·L-1的硫酸溶液;④用标准NaOH溶液滴定未知浓度的盐酸,用去18.20 mL NaOH溶液,其中数据合理的是 ( )
A.①④ B.②④ C.①③ D.②③
答案 A
解析 解此题的关键在于依据所用仪器的精确度,如实记录可测得的可靠数值。托盘天平称量物质的精确度为0.1 g,①正确;量筒量取液体体积的精确度为0.1 mL,②错误;容量瓶的规格中有100 mL、250 mL、500 mL、1 000 mL等,没有210 mL的,③错误;中和滴定要用滴定管,滴定管的精确度为0.01 mL,18.20 mL的数值合理,④正确。
6.某同学用托盘天平称量烧杯的质量,天平平衡后的状态如下图,由图中可以看出,该同学在操作时的一个错误是________________________。烧杯的实际质量为__________ g。

答案 砝码放在左盘,被称物放在右盘 27.4
7.(1)下图为常见仪器的部分结构(有的仪器被放大)


A图中液面所示溶液的体积为_____mL,C图中液面所示溶液的体积为____mL,用上述四种仪器中的某种测量一液体的体积,平视时读数为N mL,仰视时读数为M mL,若M>N,则所使用的仪器是_______(填仪器序号字母)。
(2)粗盐经提纯后得到NaCl溶液,再经蒸发、结晶、烘干得精盐。
①蒸发操作中使用到的瓷质仪器的名称为__________。
②该同学将所得精盐配成溶液,用于另一实验。实验中需要用100 mL 1 mol·L-1的NaCl溶液,配制过程中需用托盘天平称取的精盐质量为______g,用于配制该准确浓度溶液的玻璃仪器的规格和名称_______________。
答案 (1)28.0 21.30 C;(2)①蒸发皿 ②5.9 100 mL容量瓶
解析 (1)A图小刻度在下面,A图是量筒,每一刻度是1.0 mL,则图中液面所示溶液的体积为28.0 mL;C图小刻度在上面,C图是滴定管,每一刻度是0.10 mL,则图中液面所示溶液的体积为21.30 mL;测量一液体的体积,平视时读数为N mL,仰视时读数为M mL,若M>N,说明小刻度在上面,该仪器为C(滴定管)。(2)①蒸发中使用到的瓷质仪器为蒸发皿;②精盐质量为0.1 L×1 mol·L-1×58.5 g·mol-1≈5.9 g;用于配制准确浓度溶液的玻璃仪器为容量瓶。
8.下图是几种常见的加热装置。
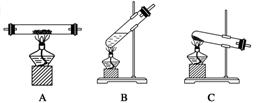
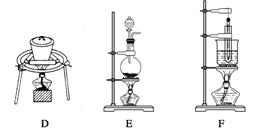
(1)A、B、C、D四装置都是用酒精灯直接加热,E、F装置加热时需垫_______。其中F装置中对试管的加热方式是_____,采用这种加热方式的目的是____。
(2)H2还原CuO可选用________装置。
(3)NH4Cl与Ca(OH)2混合制NH3可选用_________装置。
(4)胆矾中结晶水含量的测定可选用________装置。
(5)乙酸乙酯的制备可选用________装置。
(6)MnO2与浓盐酸混合制氯气可选用________装置。若该装置只加热液体时,容器内必须放____________________。
答案 (1)石棉网 水浴加热 使仪器受热均匀,便于控制溶液的温度
(2)A (3)C (4)D (5)B (6)E 碎瓷片或沸石
9.无水氯化铝是白色晶体,易吸收水分,在178 ℃升华,装有无水氯化铝的试剂瓶久置于潮湿的空气中,会自动爆炸产生大量白雾。如图是实验室制取少量无水AlCl3的部分装置,其中Cl2是由MnO2和浓盐酸反应制取的,请回答下列问题:
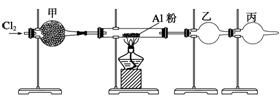
(1)甲装置所盛试剂(足量)可能是__________。
(2)由MnO2和浓盐酸反应制得的Cl2中可能含两种杂质气体,而甲装置只能除去其中一种,另一种杂质气体是否有必要除去,原因是___________;如必须除去,还需在上图中加何种装置__________。
(3)装置图中乙、丙两支干燥管中需要填充碱石灰的是________(填“乙”、“丙”或“乙、丙”),乙的作用是____________,丙的作用是__________。
答案 (1)P2O5或CaCl2 (2)必须除去,HCl与Al反应会产生H2,H2与Cl2混合加热爆炸 可在甲装置前加一盛饱和食盐水的洗气瓶
(3)丙 吸收无水AlCl3 吸收未反应的Cl2,防止空气中的水蒸气进入乙中
1.变换思维角度——广口瓶的“一材多用”
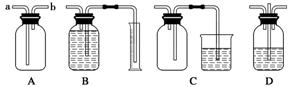
要注意广口瓶的不同用途中,导气管的长短不同。
(1)A装置可作集气瓶和洗气瓶
例如,利用A装置收集或干燥以下三种气体。
①Cl2 ②NH3 ③NO
Ⅰ.若集气瓶是干燥的,则由b口进气可收集的气体有②。
Ⅱ.若集气瓶是干燥的,则由a口进气可收集的气体有①。
Ⅲ.若集气瓶充满水,可收集的气体有③;此时气体由b口进入。
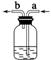 Ⅳ.若集气瓶内装入浓硫酸进行气体干燥,可用此装置干燥的气体是①③,这时气体由a口进入。
Ⅳ.若集气瓶内装入浓硫酸进行气体干燥,可用此装置干燥的气体是①③,这时气体由a口进入。
(2)A装置用于监控气体流速
例如:给病人输氧气时,可在广口瓶中加入少量水,从a端通入氧气,b端接入呼吸
罩,则可从广口瓶中产生气泡的速率来监控所通氧气的速率(如图)。
(3)测量气体的体积(B装置)
长导管与另一弯管连接伸入量筒底部,广口瓶中盛满水,气体“短进长出”。将广口瓶中的水排到量筒中来测量难溶于水的气体的体积。
(4)安全防倒吸装置
①C装置中长导管与另一弯管连接伸入溶液中,气体“短进长出”。
②D装置中,两短导管间加一长直玻璃管,气体从两短导管其中一个进,另一个出。
2.球形干燥管——多变的角色
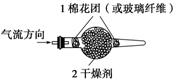
①干燥管内盛无水硫酸铜时,可用于水的检验。
②可用于有毒气体的尾气吸收,如内盛碱石灰可吸收HCl、Cl2、SO2等。
③可用于定量测定气体的质量。定量测定时,有时需要考虑空气中的成分对测定的影响,所以吸收气体的装置后还要另接一个干燥管,目的是防止空气中的水或二氧化碳等对定量测定产生干扰。
【教后记】
相关热词搜索:
上一篇:第13单元 化学实验.ppt
下一篇:第十三单元 化学实验(2)


