�ڰ˵�Ԫ ��ѧ��Ӧ��������1��
2015-11-19 09:33:44 ��Դ�� �壺��Х ��Ӱ���� ; ���ۣ�0 �����
�ڰ˵�Ԫ ��ѧ��Ӧ��������1��
|
|
|
�ڿ��ˣ��� Х |
|
|
�����շ�Ӧ�ȡ�ȼ���Ⱥ��к��ȵ���Ҫ��� |
|
|
��ѧĿ�꣺ |
�������к��Ȳⶨ�ķ��������ݴ����������˽������������� |
|
|
|
�������Ȼ�ѧ����ʽ�ĸ����ȷ��д�Ȼ�ѧ����ʽ�� |
|
|
��ѧ�ص㣺 |
��Ӧ�ȼ��� |
|
|
��ѧ�ѵ㣺 |
��˹���ɵ�Ӧ�� |
|
|
��ѧ������ |
�����ȽϷ� |
|
|
��ѧ���̣� |
|
|
����֪ʶ����
һ����Ӧ��
1.��ѧ��Ӧ�Ļ���������
��Ӧ�������������ɣ�ͬʱ�������������仯��ͨ������Ϊ�����ı仯��
2.��Ӧ�ȣ�
�ڻ�ѧ��Ӧ�����ջ�ų��������ͽз�Ӧ�ȡ���������H��ʾ����λkJ��mol��
3.���ȷ�Ӧ�����ȷ�Ӧ
��ѧ�ϰ��������ų��ķ�Ӧ�������ȷ�Ӧ�������������Ļ�ѧ��Ӧ�������ȷ�Ӧ����H>OΪ���ȷ�Ӧ����H<OΪ���ȷ�Ӧ��
4����Ӧ�ȵļ�����ж�
���ڷ�Ӧ�ȱ�ʾ���ǻ�ѧ��Ӧ��������ϵ�����ı仯��������Է�Ӧ�������¼����жϺͼ��㷽����
������������������жϣ�
��ѧ��Ӧ�������Ȼ��Ƿ�����Ҫȡ���ڷ�Ӧ������������������������ĸߵ͡�
��Ӧ�ȵ������������������ȥ��Ӧ�����������
��H=E(������������)��E(��Ӧ��������)

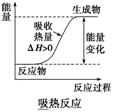
����Ӧ��������������������������������Ӧʱ������һ����������������ͷų����������ȷ�Ӧ��
����Ӧ�������е�����������������������������ڷ�����ѧ��Ӧʱ����Ӧ�����Ҫ������������ת��Ϊ����������ȷ�Ӧ��
�����������仯������ж�
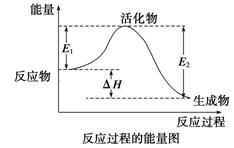
��Ӧ�ȵ����ƻ���Ӧ�����յ�������ȥ����������ų���������
��H=E1- E2
���ƻ���Ӧ�����յ�����С�ڲ���������ų���������Ϊ���ȷ�Ӧ��
���ƻ���Ӧ�����յ��������ڲ���������ų���������Ϊ���ȷ�Ӧ��
�����û�ѧ��������жϣ�
��Ӧ�ȵ��ڷ�Ӧ����ܼ��ܼ�ȥ��������ܼ��ܡ�
��H=E(��Ӧ���ܼ���)��E(�������ܼ���)
����Ӧ����ܼ��ܴ�����������ܼ���ʱ���ȷ�Ӧ��
����Ӧ����ܼ���С����������ܼ���ʱ���ȷ�Ӧ��
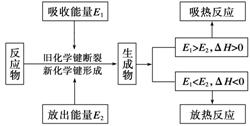
5.�����ķ��ȷ�Ӧ�����ȷ�Ӧ
���������ȷ�Ӧ��
��ȼ���ȼ�գ�����кͷ�Ӧ����������Ϸ�Ӧ������������û���Ӧ�����ʵĻ���������
���������ȷ�Ӧ��
������ֽⷴӦ���ε�ˮ���������ʵĵ��룻Ba(OH)2��8H2O��NH4Cl��Ӧ��̼��ˮ������C��CO2�ķ�Ӧ��
![]() ���˼��
���˼��![]()
1��ͬ����������ڿ�����ȼ�պ��ڴ�����ȼ�գ���һ���ų��������࣬Ϊʲô��
�𰸡��ڿ�����ȼ�շų��������࣬���ڴ�����ȼ�ջ���������ת���ɵĹ��ܶ࣬�ʷų��������١�
2���ж�������ȷ�Ļ�������������Ļ�������
(1)���ȷ�Ӧ����Ҫ���Ⱦ��ܷ�Ӧ�����ȷ�Ӧ�����ȾͲ��ܷ�Ӧ (����)
(2)���ʷ�����ѧ�仯�����������ı仯 (����)
(3)���������仯�����ʱ仯���ǻ�ѧ�仯 (����)
(4)���ȷ�Ӧ���κ����������ܷ��� (����)
(5)Naת��ΪNa��ʱ�����յ��������Ǹù��̵ķ�Ӧ�� (����)
(6)ˮ������ΪҺ̬ˮʱ�ų����������Ǹñ仯�ķ�Ӧ�� (����)
����(1)����(2)����(3)����(4)����(5)����(6)��
������(5)(6)�������仯���̣��������仯���ܳ�Ϊ��Ӧ�ȡ�
�����Ȼ�ѧ����ʽ
1�����
����ʾ��Ӧ���ų������������Ļ�ѧ����ʽ�������Ȼ�ѧ����ʽ��
����ʾ���뻯ѧ��Ӧ�����ʵ����ʵ����ͷ�Ӧ�ȵĹ�ϵ�Ļ�ѧ����ʽ��
2����ʾ���壺
���������˻�ѧ��Ӧ�е����ʱ仯��Ҳ�����˻�ѧ��Ӧ�е������仯��
3����д������д���̡���״̬����������
��ע�⡿
��������H����ֵ�������ţ�ע����Ӧ�������ľۼ�״̬(s��l��g��aq)��
����ѧʽǰ�ļ������������������������H����ֵ�뻯ѧʽǰ�������йأ���H����ֵ�뷴Ӧ����ʽ�л�ѧʽǰ��Ļ�ѧ�������ɱ������������ӱ�����H��ֵҲҪ�ӱ�����λ����kJ��mol��
��ע���ⶨ��������Ϊ25����1.01��105Pa�ɲ�ע����
![]() ���˼��
���˼��![]()
1����H�ĵ�λ��kJ��mol��1���ĺ�����ʲô��
������kJ��mol��1��������ָÿĦ���������ʷ�Ӧʱ����������仯������ָ������ʽ�ľ��巴Ӧ�������仯����2H2(g)��O2(g)===2H2O(g)����H����483.6 kJ��mol��1���˷�Ӧ�ķ�Ӧ����ָÿĦ����Ӧ[2H2(g)��O2(g)===2H2O(g)]�ų�������Ϊ483.6 kJ����H�뻯ѧ��Ӧ����ʽ��д���йأ���H2(g)��O2(g)===H2O(g)����H����241.8 kJ��mol��1�����ⷴӦ�Ȼ��뷴Ӧ���״̬�йأ���2H2(g)��O2(g)===2H2O(l)����H����571.6 kJ��mol��1��
2������������淴Ӧ�еķ�Ӧ�ȣ�
�������ۻ�ѧ��Ӧ�Ƿ���棬�Ȼ�ѧ����ʽ�еķ�Ӧ����H����ʾ��Ӧ���е���(��ȫת��)ʱ�������仯����2SO2(g)��O2(g)���2SO3(g)����H����196.64 kJ��mol��1����H��ָ2 mol SO2(g)��1 mol O2(g)��ȫת��Ϊ2 mol SO3(g)ʱ�ų���������������ͬ���¶Ⱥ�ѹǿ�£���ij�����м���2 mol SO2(g)��1 mol O2(g)����Ӧ�ﵽƽ��ʱ�ų�������ΪQ����Ӧ������ȫת��ΪSO3(g)����Q<196.64 kJ��
3��ʵ������4 mol SO2��2 mol O2��һ�������½������з�Ӧ��2SO2(g)��O2(g)=2SO3(g)����H����196.64 kJ��mol��1�����ų�314.624 kJ����ʱ��SO2��ת����Ϊ________��
�𰸡�80%
4�������
�Ȼ�ѧ����ʽ�������ж���һ���������ͣ�ͨ���жϷ��������忴����
(1) �������ʵľۼ�״̬�Ƿ���ȷ��
(2) ����H���������������������Ƿ���ȷ��
(3) ����Ӧ�ȵ���ֵ�뻯ѧ�������Ƿ��Ӧ��
(4)������ʽ�Ƿ���ƽ��
(5) ����Ӧ�ȵĵ�λ�Ƿ�ΪkJ��mol��1��
����ȼ���Ⱥ��к���
1��ȼ����
�������101kPaʱ��lmol������ȫȼ�������ȶ���������ʱ���ų������������������ʵ�ȼ���ȣ���λΪkJ��mol��
����ȫȼ��������ָ����������Ԫ����ȫת��ɶ�Ӧ�������C��CO2(g)��H��H2O(l)��S��SO2(g)�ȡ�
���磬��̼ȼ������һ����̼�ķ�Ӧ������ȼ������ˮ�����ķ�Ӧ��Ӧ�ķ�Ӧ�ȶ�������ȼ���ȡ�
����ʾ���壺
���磺C��ȼ����Ϊ393.5 kJ��mol����ʾ��101 kPaʱ��1molC��ȫȼ�շų�393��5 kJ��������
����д�Ȼ�ѧ����ʽ��
ȼ��������1 mol������ȫȼ�����ų�������������ģ������д��ʾȼ���ȵ��Ȼ�ѧ����ʽʱӦ��ȼ��1mol����Ϊ������ƽ�������ʵĻ�ѧ��������
C8H18(l)��O2(g)===8CO2(g)��9H2O(l)����H����5 518 kJ��mol��1����C8H18��ȼ����Ϊ5 518 kJ��mol��1��
���ų������ļ��㣺Q(��)=n(��ȼ��)����H
2�����
��1�����
��ϡ��Һ�У��������кͷ�Ӧ����1molH2O����ʱ�ķ�Ӧ�Ƚ��к��ȡ�
H+(aq)+OH-(aq)=H2O(1)����H=��57��3 kJ��mol
ע�⣺����������1molˮΪ�����кͷ�Ӧ�Ķ���Ϊϡ��Һ��ǿ����ǿ���к�ʱ����1molH2O������57��3kJ��������������ʱҪ�����������������Dz����кͷ�Ӧʱ���к���С��57��3 kJ��
(2)��Ҫʵ�飺�к��ȵIJⶨ
���ⶨԭ����
�ⶨһ�������������кͷ�Ӧ����H2Oʱ���ͷŵ�������ͨ�����㣬�ó�����1molH2Oʱ�ķ�Ӧ�ȣ���Ϊ�к��ȡ�
��H��
c��4.18 J��g��1������1��4.18��10��3 kJ��g��1������1��nΪ����H2O�����ʵ�����
��ʵ����̣�
��100mL�ձ��м���50mL 0.50mol/L�����ᣬ�����¶ȡ�������Ͳ��ȡ50mL0.55mol/LNaOH��Һ�������¶ȣ���һ�ε����ձ��У���ע�Ᵽ�¡��û��β��������裬�۲췴Ӧ����Һ�¶ȵı仯���̣������ü�¼��
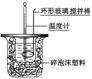
��ʵ�鲽�裺
(1)������װ��:�ڴ��ձ��ײ�����ĭ����(��ֽ��)ʹ�����С�ձ���������ձ�������ƽ��Ȼ�����ڴ�ˮ�ձ�֮��������ĭ���ϡ�
(2)��ȡ��Ӧ���������������¶�:����ȡ50 mL��50 mol��L-1���ᣬ����С�ձ��У����¶ȼƲ���������¶ȡ�Ȼ������ȡ50 mL 0.50mol��L-1 NaOH��Һ�����¶ȼƲ������¶ȡ�
(3)������Ӧ����¶�:���¶ȼƺͻ��β���������С�ձ��������У�������Ͳ�е�NaOH��Һһ�ε���С�ձ��С����������Һ����ȷ��ȡ�����Һ������¶ȣ���Ϊ��ֹ�¶ȡ�
(4)�ظ�ʵ��:�ظ�ʵ�����Σ�ȡ�����������ݵ�ƽ��ֵ��Ϊ�������ݡ�
(5)�������ݼ����к��ȡ�
��ע�⡿
������Ч��һ��Ҫ�ã�С�ձ�����ձ��ı���Ҫ��ƽ��
�������NaOH��Ũ��Ҫȷ��
��������0.1�ֶȵ��¶ȼƣ��¶ȼ�ˮ����Ӧ��û����Һ�С�
����ȡ��Ӧ�¶�ʱҪ����ϸ�£�������¶ȡ�
![]() ���˼��
���˼��![]()
1��װ��������ĭ����(��ֽ��)����ĭ���ϰ��������ʲô��
�������¡����ȣ�����ʵ���������������ʧ��
2���������ܱ�֤�ᡢ����ȫ��Ӧ��
����ʹ�����Թ�����
3�������û��β��������������Һ��������ͭ˿����������������ʲô��
����ʵ��ʱӦ�û��β�����������½�������Ϊͭ���ȿ죬������ʧ�����Բ�����ͭ˿��������滷�β����������
4����ʵ�������Թ�����NaOH��ԭ��̲���˵��Ϊ��֤������ȫ���к͡����ʣ��ڷ�Ӧ������Ϊ�з��������������HCl�ڷ�Ӧ�лӷ������õ��к���________(����ƫ��������ƫС������������)��
����ƫС
���̺�ǡ�
����ѵ������Ӧ�ȵĻ������㷽��
1��ij��Ӧ��������ϵ�������仯��ͼ��ʾ������˵��������� (����)
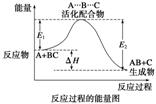
A����Ӧ���̿ɱ�ʾΪ![]()
B��E1Ϊ��Ӧ���ƽ�����������̬���������Ϊ����Ӧ�Ļ��
C������Ӧ����ЧӦΪ��H��E1��E2<0����������ӦΪ���ȷ�Ӧ
D����ͼ���淴Ӧ����ЧӦ��H��E1��E2<0�������淴ӦΪ���ȷ�Ӧ
����D
��������ͼ��ʾ������Ӧ���ȣ���HΪ��ֵ���淴Ӧ���ȣ���HΪ��ֵ��D����
2��(2011���������ۣ�13)SF6��һ�������ľ�Ե���壬���ӽṹ��ֻ����S��F������֪��1 mol S(s)ת��Ϊ��̬��ԭ����������280 kJ������1 mol F��F��S��F����Ҫ���յ������ֱ�Ϊ160 kJ��330 kJ����S(s)��3F2(g)===SF6(g)�ķ�Ӧ����HΪ________��
������1 220 kJ��mol��1
����������1 mol S��S����������280 kJ������3 mol F��F����������3��160 kJ�������յ�������ΪQ����280 kJ��3��160 kJ��760 kJ���ͷŵ�������ΪQ����330 kJ��6��1 980 kJ���ɷ�Ӧ����ʽ��S(s)��3F2(g)===SF6(g)��֪����H��760 kJ��mol��1��1 980 kJ��mol��1����1 220 kJ��mol��1��
3��ͨ���Ѳ�1 molij��ѧ�������յ��������ɸû�ѧ���ļ��ܡ����ܵĴ�С���Ժ�����ѧ����ǿ����Ҳ�����ڹ��㻯ѧ��Ӧ�ķ�Ӧ��(��H)����ѧ��Ӧ����H���ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ�����о���һЩ��ѧ���ļ������ݣ�������ʹ�á�
|
��ѧ�� |
Si��O |
Si��Cl |
H��H |
H��Cl |
Si��Si |
Si��C |
|
����/kJ��mol��1 |
460 |
360 |
436 |
431 |
176 |
347 |
��ҵ�ϵĸߴ����ͨ�����з�Ӧ��ȡ��SiCl4(g)��2H2(g)===Si(s)��4HCl(g)���÷�Ӧ�ķ�Ӧ��(��H)Ϊ________��
������236 kJ��mol��1
������SiCl4��H2��HCl�����й��ۼ�����Ŀ�����㣬�����������ԭ�Ӿ��壬�ɸ���ԭ�Ӿ���Ľṹ���㾧����еĹ��ۼ�����Ŀ��1 mol�������������Si��Si��Ϊ2 mol������ȡ�ߴ��跴Ӧ�ķ�Ӧ����H��4��360 kJ��mol��1��2��436 kJ��mol��1��(2��176 kJ��mol��1��4��431 kJ��mol��1)����236 kJ��mol��1��
����һ���Ȼ�ѧ����ʽ����д
1��������ʵ��д�����з�Ӧ���Ȼ�ѧ����ʽ��
(1)������N2��O2��ȫ��Ӧ��ÿ����23 g NO2����16.95 kJ ������N2��O2��Ӧ���Ȼ�ѧ����ʽΪ____________________��
(2)SiH4��һ����ɫ���壬���������ܷ�����ը����ȼ������SiO2��Һ̬H2O����֪������2 g SiH4��ȼ�ų�����89.2 kJ��SiH4��ȼ���Ȼ�ѧ����ʽΪ______��
(3)��֪��1 mol H��H����1 mol N��H����1 mol N��N���ֱ���Ҫ��������436 kJ��391 kJ��946 kJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ_______��
(4)��25 ����101 kPa�£�һ����������ˮ�Ҵ���ȫȼ��ʱ�ų�����Q kJ����ȼ�����ɵ�CO2�ù�������ʯ��ˮ���տɵ�100 g CaCO3���������Ҵ�ȼ�յ��Ȼ�ѧ����ʽΪ_____________��
����(1)N2(g)��2O2(g)===2NO2(g) ��H����67.8 kJ��mol��1
(2)SiH4(g)��2O2(g)===SiO2(s)��2H2O(l) ��H����1 427.2 kJ��mol��1
(3)N2(g)��3H2(g)===2NH3(g)����H����92 kJ��mol��1
(4)C2H5OH(l)��3O2(g)===2CO2(g)��3H2O(l) ��H����2Q kJ��mol��1
������(1)23 g NO2�����ʵ���Ϊ0.5 mol��������2 mol NO2���յ�����Ϊ67.8 kJ�����ȷ�Ӧ��HΪ��ֵ���ʷ�Ӧ���Ȼ�ѧ����ʽΪ��
N2(g)��2O2(g)===2NO2(g)����H����67.8 kJ��mol��1��
(2)2 g SiH4��ȼ�ų�����89.2 kJ,1 mol SiH4��ȼ�ų�����1 427.2 kJ�����Ȼ�ѧ����ʽΪSiH4(g)��2O2(g)===SiO2(s)��2H2O(l)����H����1 427.2 kJ��mol��1��
(3)N2(g)��3H2(g)===2NH3(g)����H��(946��436��3��391��6)kJ��mol��1����92 kJ��mol��1��
 (4)����Cԭ���غ�����C2H5OH��2CO2��2CaCO3������100 g CaCO3���������Ҵ�Ϊ0.5 mol���ݴ˿�д����Ӧ���Ȼ�ѧ����ʽ��
(4)����Cԭ���غ�����C2H5OH��2CO2��2CaCO3������100 g CaCO3���������Ҵ�Ϊ0.5 mol���ݴ˿�д����Ӧ���Ȼ�ѧ����ʽ��
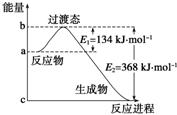
2.��ͼ��NO2��CO��Ӧ����CO2��NO�����������仯ʾ��ͼ����д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ��_______________��
����NO2(g)��CO(g)===CO2(g)��NO(g)����H����234 kJ��mol��1
��������ͼ��֪���������������ڷ�Ӧ�����������÷�Ӧ�Ƿ��ȷ�Ӧ����H��E1��E2��134 kJ��mol��1��368 kJ��mol��1����234 kJ��mol��1��
��������Ȼ�ѧ����ʽ���ж�
3��ʵ���ã�101 kPaʱ��1 mol H2��ȫȼ������Һ̬ˮ���ų�285.8 kJ��������1 mol CH4��ȫȼ������Һ̬ˮ��CO2���ų�890.3 kJ�������������Ȼ�ѧ����ʽ����д��ȷ���� (����)
��CH4(g)��2O2(g)===CO2(g)��2H2O(l) ��H����890.3 kJ��mol��1
��CH4(g)��2O2(g)===CO2(g)��2H2O(l) ��H����890.3 kJ��mol��1
��CH4(g)��2O2(g)===CO2(g)��2H2O(g) ��H����890.3 kJ��mol��1
��2H2(g)��O2(g)===2H2O(l) ��H����571.6 kJ��mol��1
A�������� B�������ڢ�
C�������ڢۢ� D��ȫ������Ҫ��
����B
4�������Ȼ�ѧ����ʽ��д��ȷ����(��H�ľ���ֵ����ȷ) (����)
A��S(s)��O2(g)===SO3(g) ��H����315 kJ��mol��1(ȼ����)
B��NaOH(aq)��HCl(aq)===NaCl(aq)��H2O(l) ��H����57.3 kJ��mol��1(���)
C��C2H5OH��3O2===2CO2��3H2O ��H����1 368.8 kJ��mol��1(��Ӧ��)
D��2H2O(g)===2H2(g)��O2(g) ��H����483.6 kJ��mol��1(��Ӧ��)
����B
����һ��ȼ���ȡ��к��ȵĺ��弰����
1����֪��Ӧ��
��101 kPaʱ��2C(s)��O2(g)===2CO(g)����H����221 kJ��mol��1
��ϡ��Һ�У�H��(aq)��OH��(aq)===H2O(l)����H����57.3 kJ��mol��1��
���н�����ȷ���� (����)
A��̼��ȼ���ȴ���110.5 kJ��mol��1
B����Ӧ���ķ�Ӧ��Ϊ221 kJ��mol��1
C��98%��Ũ������ϡ����������Һ��Ӧ����1 molˮ���к���Ϊ��57.3 kJ��mol��1
D��ϡ������ϡ����������Һ��Ӧ����1 molˮʱ�ų�57.3 kJ������
����A
2�����й����Ȼ�ѧ��Ӧ����������ȷ���� (����)
A����֪H��(aq)��OH��(aq)===H2O(l)����H����57.3 kJ��mol��1����H2SO4��Ba(OH)2��Ӧ�ķ�Ӧ����H��2��(��57.3) kJ��mol��1
B��ȼ�ϵ���н��״�����ת��Ϊ�������Ȼ�ѧ����ʽ��CH3OH(g)��O2(g)===CO2(g)��2H2(g) ��H����192.9 kJ��mol��1����CH3OH(g)��ȼ����Ϊ192.9 kJ��mol��1
C��H2(g)��ȼ������285.8 kJ��mol��1����2H2O(g)===2H2(g)��O2(g)����H����571.6 kJ��mol��1
D�������ǵ�ȼ������2 800 kJ��mol��1����C6H12O6(s)��3O2(g)===3CO2(g)��3H2O(l)����H����1 400 kJ��mol��1
����D
��������к��Ȳⶨ�����������ݴ���
3��������ͼ��ʾװ�òⶨ�к��ȵ�ʵ�鲽�����£�
������Ͳ��ȡ50 mL 0.50 mol��L��1���ᵹ��С�ձ��У����������
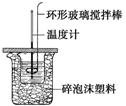 �ȣ�������һ��Ͳ��ȡ50 mL 0.55 mol��L��1 NaOH��Һ��������һ�¶ȼƲ�����¶ȣ�����NaOH��Һ����С�ձ��У��跨ʹ֮��Ͼ��ȣ���û��Һ����¶ȡ��ش��������⣺
�ȣ�������һ��Ͳ��ȡ50 mL 0.55 mol��L��1 NaOH��Һ��������һ�¶ȼƲ�����¶ȣ�����NaOH��Һ����С�ձ��У��跨ʹ֮��Ͼ��ȣ���û��Һ����¶ȡ��ش��������⣺
(1)Ϊʲô����NaOH��ҺҪ�Թ�����____________��
(2)����NaOH��Һ����ȷ������__________(�����)��
A���ز������������룻B���������������룻C��һ��Ѹ�ٵ���
(3)ʹ������NaOH��Һ��Ͼ��ȵ���ȷ������________(�����)��
A�����¶ȼ�С�Ľ���
B���ҿ�ӲֽƬ�ò���������
C����������ձ�
D���������¶ȼ��ϵĻ��β������������ؽ���
(4)�ֽ�һ������ϡ����������Һ��ϡ����������Һ��ϡ��ˮ�ֱ��1 L 1 mol��L��1��ϡ����ǡ����ȫ��Ӧ���䷴Ӧ�ȷֱ�Ϊ��H1����H2����H3������H1����H2����H3�Ĵ�С��ϵΪ________________��
(5)�������������������Һ���ܶȶ���1 g��cm��3����֪�кͷ�Ӧ��������Һ�ı�����c��4.18 J��g��1������1��Ϊ�˼����к��ȣ�ijѧ��ʵ���¼�������£�
|
ʵ����� |
��ʼ�¶�t1/ �� |
��ֹ�¶�t2/ �� |
|
|
���� |
����������Һ |
�����Һ |
|
|
1 |
20.0 |
20.1 |
23.2 |
|
2 |
20.2 |
20.4 |
23.4 |
|
3 |
20.5 |
20.6 |
23.6 |
���ݸ�ѧ����ʵ�����ݼ��㣬��ʵ���õ��к�����H��__________(�������һλС��)��
(6)________(������������������)��Ba(OH)2��Һ�������������������Һ�����ᣬ������_____________________________________��
����(1)ȷ�����ᱻ��ȫ�к͡�(2)C��(3)D��(4)��H1����H2<��H3��
(5)��51.8 kJ��mol��1��(6)���ܡ�H2SO4��Ba(OH)2��Ӧ����BaSO4�����������Ȼ�Ӱ�췴Ӧ�ķ�Ӧ��
������(1)���к��ȵIJⶨʵ����Ϊ��ȷ����Ӧ�ﱻ��ȫ�кͣ�����ʹ�����һ�ַ�Ӧ��������һЩ��
(2)Ϊ�˼�С������ʧ������NaOH��ҺӦ��һ��Ѹ�ٵ��롣
(3)ʹ������NaOH��Һ��Ͼ��ȵ���ȷ�������������¶ȼ��ϵĻ��β������������ؽ�����
(4)ϡ����������Һ��ϡ����������Һ�����ʶ���ȫ���룬���ǵ��к�����ͬ��ϡ��ˮ�е�������������ʣ���������ķ�Ӧ��һˮ�ϰ��ĵ���Ҫ�������������к���ҪСһЩ(ע���к�������H�Ĺ�ϵ)��
(5)ȡ����ʵ���ƽ��ֵ���빫ʽ���㼴�ɡ�
(6)��Ϊ������Ba(OH)2��Һ��Ӧ����BaSO4�����������Ȼ�Ӱ�췴Ӧ�ķ�Ӧ�ȣ��ʲ�����Ba(OH)2��Һ�������������������Һ�����ᡣ
����ȴ�������
��һƪ�����ߵ�Ԫ ���ʽṹ Ԫ�������ɣ�5��
��һƪ���ڰ˵�Ԫ ��ѧ��Ӧ��������2��
