�ڰ˵�Ԫ ��ѧ��Ӧ��������2��
2015-11-19 09:37:42 ��Դ�� �壺��Х ��Ӱ���� ; ���ۣ�0 �����
�ڰ˵�Ԫ ��ѧ��Ӧ��������2��
|
|
|
�ڿ��ˣ��� Х |
|
|
�����շ�Ӧ�ȡ�ȼ���Ⱥ��к��ȵ���Ҫ��� |
|
|
��ѧĿ�꣺ |
�������к��Ȳⶨ�ķ��������ݴ����������˽������������� |
|
|
|
�������Ȼ�ѧ����ʽ�ĸ����ȷ��д�Ȼ�ѧ����ʽ�� |
|
|
��ѧ�ص㣺 |
��Ӧ�ȼ��� |
|
|
��ѧ�ѵ㣺 |
��˹���ɵ�Ӧ�� |
|
|
��ѧ������ |
�����ȽϷ� |
|
|
��ѧ���̣� |
|
|
����֪ʶ����
�ġ���Ӧ�ȼ���
1����˹����
�ٻ�ѧ��Ӧ�ķ�Ӧ��ֻ�뷴Ӧ��ʼ̬������Ӧ�����̬����������йأ�������巴Ӧ���е�;���ء�
�ڻ�ѧ��Ӧ������һ����ɻ��Ƿּ�����ɣ����ܵķ�Ӧ������ͬ�ġ�
˵������������˹���������ֱ�����ʽ����ʵ������ͬ�ġ�
[����]
���κλ�ѧ��Ӧ�ķ�Ӧ�Ⱥ����淴Ӧ�ķ�Ӧ�ȴ�С��ȣ������෴��
���κλ�ѧ��Ӧ����������ϵ�������仯ʱ����Ӧ�ȵ���ֵҲ��֮������ͬ�仯��
��H=��H1+��H2+��H3 ��H��=����H��
������ָ�������õ�ʽ�ĺ�ȱ��ε�˼·�����ȹ۲���Ҫ�����Ŀ�껯ѧ��Ӧ�ķ���ʽ�����ݸ÷�Ӧ�ķ�Ӧ�Pϵ��������֪���Ȼ�ѧ����ʽ���������Ӧ��ϵ������Ӧ��Ҳͬʱ�������㣩��Ȼ����мӼ��ϲ������ָ��������ʹ�ϲ���ķ���ʽ���������ߺ�Ŀ�껯ѧ��Ӧ�ķ���ʽ��ȫ��ͬ���������õķ�Ӧ�ȵ���ֵ��������Ӧ�ķ�Ӧ�ȣ����õĵ�ʽ��������Ļ�ѧ��Ӧ���Ȼ�ѧ����ʽ��
���⡢��֪����CH4(g)+2O2(g)��CO2(g)+2H2O(l)����H1=-890.3kJ��mol-1;
��C(ʯī)+O2(g)��CO2(g)����H2=-393��5kJ��mol-1
��H2��g��+![]() O2��g��=H2O��l������H3=-285.8kJ��mol-1
O2��g��=H2O��l������H3=-285.8kJ��mol-1
ʵ���в���ֱ�Ӳ����ʯī���������ɼ��鷴Ӧ�Ħ�H������㷴Ӧ��C(ʯī)+2H2(g)��CH4(g)�ķ�Ӧ�Ȧ�H��
�ɷ���ʽC(ʯī)+2H2(g)��CH4(g)��֪��ͨ����+�ۡ�2���ٿ��Եõ��÷���ʽ����˸÷�Ӧ�ķ�Ӧ��Ϊ��
��H=��H2+2��H3-��H1
=-393.5kJ��mol-1+2(-285.8) kJ��mol-1��(-890.3) kJ��mol-1
=��74.8kJ��mol-1
2����H�ıȽ�
�Ƚ���H�Ĵ�Сʱ�迼�������ţ��Է��ȷ�Ӧ������Խ�࣬��HԽС�������ȷ�Ӧ������Խ�࣬��HԽ��
3����Ӧ�ȼ���
(1)�����Ȼ�ѧ����ʽ���㣺
��Ӧ���뷴Ӧ������ʵ��������ȡ�
(2)���ݸ�˹��������
Ӧ�ø�˹���ɽ��м���ʱ���ؼ������ȵó���Ҫ���Ȼ�ѧ����ʽ��
ע�⣺
������Ŀ���Ȼ�ѧ����ʽ�����ԭ�Ȼ�ѧ����ʽ(һ��2��3��)���к��������������Ȼ�ѧ����ʽ�ߵ����˳���ijһ������Ȼ��������ӡ������õ�Ŀ���Ȼ�ѧ����ʽ�����Ŀ���Ȼ�ѧ����ʽ����H��ԭ�Ȼ�ѧ����ʽ֮����H�Ļ����ϵ��
�����Ȼ�ѧ����ʽ�ˡ�����ijһ����ʱ����HҲӦ��Ӧ�سˡ�����ijһ����������ʽ���мӼ�����ʱ����HҲͬ��Ҫ���мӼ����㣬��Ҫ�����������������ţ�������H����һ������������㡣
����һ���Ȼ�ѧ����ʽ�ߵ���дʱ����H�ķ���Ҳ��֮�ı䣬����ֵ���䡣
������Ʒ�Ӧ�����У�������ͬһ���ʵ���̬(�̡�Һ����)���ת����״̬�ɹ���Һ�����仯ʱ�������ȣ���֮����ȡ�
![]() ���˼��
���˼��![]()
�ԱȽ�����������H�Ĵ�С
(1)ͬһ��Ӧ��������״̬��ͬʱ
A(g)��B(g)===C(g)����H1<0
A(g)��B(g)===C(l)����H2<0
��H1____��H2(����>������<��������������ͬ)��
����>
��������ΪC(g)===C(l)����H3<0
����H3����H2����H1����H2<��H1��
(2)ͬһ��Ӧ����Ӧ��״̬��ͬʱ
S(g)��O2(g)===SO2(g)����H1<0
S(s)��O2(g)===SO2(g)����H2<0
����H1____��H2��
����<
������![]()
��H2����H3����H1������H3����H1����H2������H3<0��������H1<��H2��
(3)��������ϵ�IJ�ͬ��Ӧ���
C(s)��O2(g)===CO2(g)����H1<0
C(s)��O2(g)===CO(g)����H2<0
����H1____��H2��
����<
���������ݳ�ʶ��֪CO(g)��O2(g)===CO2(g)����H3<0������Ϊ��H2����H3����H1��������H2>��H1��
�塢��Դ
1������
���ṩ��������Ȼ��Դ��
2����չ��
���ʱ������ʯ��Դʱ��������Դ�ṹʱ�ڡ�
3������
(1)��ʯȼ��
�����ࣺú��ʯ�͡���Ȼ����
���ص㣺�̲������ޣ��Ҳ���������
(2)����Դ
�����ࣺ̫���ܡ����ܡ����ܡ������ܡ������ܺ��������ܵȡ�
���ص㣺��Դ�ḻ������������û����Ⱦ����Ⱦ��С��
4����Դ����
(1)�ҹ�Ŀǰʹ�õ���Ҫ��Դ�ǻ�ʯȼ�ϣ����ǵ��̲������ޣ����Ҳ������������ս���ݽߡ�
(2)��ʯȼ�ϵĴ���ʹ�ô������صĻ�����Ⱦ���⡣
5�������Դ����Ĵ�ʩ
(1)�����Դ��ʹ��Ч��
�����ƿ��ɡ����䡢�ӹ��ȸ������ڡ�
����ѧ����ȼ�շ�Ӧ��ʹȼ�ϳ��ȼ�ա�
һ�DZ�֤ȼ��ʱ���ʵ������Ŀ�������������������O2Ũ�ȵȡ�
���DZ�֤ȼ����������㹻��ĽӴ�������罫�������ɷ�ĩ��ʹҺ�������״�ȡ�
(2)�����µ���Դ
������Դ�ḻ������������û����Ⱦ����Ⱦ��С������Դ��
![]() ���˼��
���˼��![]()
1��2009��籾���������ᣬ�DZ��������������ȵ�������һ�λ����������Ϲ�����仯��ᡣ���д�ʩ�����ڽ��ܼ��š����ƻ����������� (����)
�����������÷��������ϡ�������ֽ��Ʒ����������Դ
����չ��̼���á�ѭ�����ã������ƹ�̫���ܡ�ˮ�ܡ����ܵ���Դ������ú��ʯ�͵Ȼ�ʯȼ�ϵ�ʹ�á���ʹ��������δ��������������������ƹ�ʹ��ȼú������������SO2��Ⱦ�������ƿ�������ȼ�ϵ�����������ٻ�����β����Ⱦ
A���٢ڢܢ� B���٢ڢ� C���٢ڢۢ� D���ۢܢ�
����A
������δ���������������ʹ���������Ĵ�ʩ������Ⱦ�������������Դ�˷ѣ�������ȷ��
2����Դ��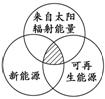 �����ͼ����ͼ��ʾ����������ѡ���У�ȫ������ͼ����Ӱ���ֵ���Դ�� (����)
�����ͼ����ͼ��ʾ����������ѡ���У�ȫ������ͼ����Ӱ���ֵ���Դ�� (����)
A��ú̿��ʯ�͡����� B��ˮ�ܡ������ܡ���Ȼ��
C��̫���ܡ����ܡ���ϫ�� D�������ܡ������ܡ�����
����C
��̽���߿���
1���ж�������ȷ�Ļ����̡�������Ļ�������
(1)ʹ��̫������ˮ�������������á��������Ҵ����漰���������ܵ����� (��)(2009���㽭���ۣ�7C)
������̫������ˮ����ʹ�ò������������ܵ����á�
(2)ʯ�͡�ú����Ȼ������ȼ����ֲ���Ͷ����ڻ�ʯȼ�� (��)(2009���㽭���ۣ�7D)
������ֲ���Ͳ����ڻ�ʯȼ�ϡ�
(3)�������ܡ�̫���ܵ�����Դ���ƹ�״����ͣ�ʹ������ϴ�Ӽ�����ֱ�ӽ���̼�ŷ� (��)(2010���㽭���ۣ�7B)
����������ϴ�Ӽ���̼���ŷŲ���ء�
(4)����ı�ȼ����Ϊ��890.3kJ��mol��1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪCH4(g)��2O2(g)===CO2(g)��2H2O(g)����H����890.3 kJ��mol��1 (��)(2010���㽭���ۣ�12A)
������ˮ��״̬����
(5)500 ����300 MPa�£���0.5 mol N2��1.5 mol H2�����ܱ������г�ַ�Ӧ����NH2(g)������19.3 kJ�����Ȼ�ѧ����ʽΪN2(g)��3H2(g)����500 �桢30 MPa2NH3(g)����H����38.6kJ��mol��1(��)(2010���㽭���ۣ�12B)
�������ϳɰ���ӦΪ���淴Ӧ����������ȫת����
(6)��ѧ��Ӧ�����������ɣ�����ѭ�����غ㶨�ɺ������غ㶨��(��)(2011���㽭���ۣ�7A)
��������ѧ�仯��ѭ�����������غ㡣
(7)ʵ���û�����(l)������ϩ(l)�ͱ�(l)�ı�ȼ���ȷֱ�Ϊ��3 916 kJ��mol��1����3 747 kJ��mol��1�ͣ�3 265 kJ��mol��1������֤���ڱ������в����ڶ�����̼̼˫��(��)(2011���㽭���ۣ�12C)
�������ɸ�˹���ɣ����ݻ�����ͻ���ϩ��ȼ���ȣ���1 mol������ʧȥ2 mol H��1 mol H2ȼ�յķ�Ӧ��֮��Ϊ��3 916 kJ��mol��1��3 747 kJ��mol��1����169 kJ��mol��1�����ݻ�����ͱ���ȼ���ȣ���1 mol������ʧȥ6 mol H��3 mol H2ȼ�յķ�Ӧ��֮��Ϊ��3 916 kJ��mol��1��3 265 kJ��mol��1����651 kJ��mol��1�����������д��ڶ�����̼̼˫�����������ķ�Ӧ��֮��Ϊ1��3������Ȼ���ߵķ�Ӧ��֮�Ȳ�Ϊ1��3��˵���������в����ڶ�����̼̼˫����
(8)��֪��Fe2O3(s)��3C(ʯī)===2Fe(s)��3CO(g) ��H��489.0 kJ��mol��1
CO(g)��O2(g)===CO2(g) ��H����283.0 kJ��mol��1
C(ʯī)��O2(g)===CO2(g) ��H����393.5 kJ��mol��1
��4Fe(s)��3O2(g)===2Fe2O3(s) ��H����1 641.0 kJ��mol��1(��)
(2011���㽭������12D)
���������ø�˹���ɣ�����������Ӧ��6����һ����Ӧ��2���ڶ�����Ӧ��6���ɵ�Ŀ�귴Ӧ������H����393.5 kJ��mol��1��6��489.0 kJ��mol��1��2��(��283.0 kJ��mol��1)��6����1 641.0 kJ��mol��1��
(9)����̫�����ڴ��������·ֽ�ˮ�����ǰѹ���ת��Ϊ��ѧ�ܵ���ɫ��ѧ����(��) (2012���㽭���ۣ�7A)
2��(2012���������ۣ�12)��(H2NNH2)��һ�ָ���ȼ�ϣ��йػ�ѧ��Ӧ�������仯����ͼ��ʾ����֪����1 mol��ѧ�����������(kJ)��N��NΪ942��O===OΪ500��N��NΪ154�������1 mol N��H�����������(kJ)�� (����)
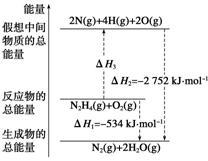
A��194 B��391 C��516 D��658
����B
3��(2012�����ȫ������9)��Ӧ A��B�D��C(��H��0)���������У���A��B��X (��H ��0)����X��C(��H��0)������ʾ��ͼ�У�����ȷ��ʾ�ܷ�Ӧ�����������仯����(����)
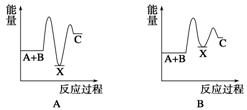
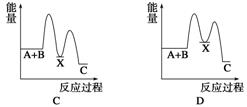
����D
���������ݷ�Ӧ��������������ĸߵ���������������⡣��ѧ��Ӧ�����������仯������Ӧ��������������������������ʱ���÷�ӦΪ���ȷ�Ӧ������Ӧ��������������������������ʱ���÷�ӦΪ���ȷ�Ӧ����Ӧ������H>0��Ϊ���ȷ�Ӧ���ʿ��ų�A���C���Ӧ������H<0��Ϊ���ȷ�Ӧ��B�����ѡD��
4��(2010���α�ȫ������11)��֪��HCN(aq)��NaOH(aq)��Ӧ����H����12.1 kJ��mol��1��HCl(aq)��NaOH(aq)��Ӧ����H����55.6 kJ��mol��1����HCN��ˮ��Һ�е������H����(����)
A����67.7 kJ��mol��1 B����43.5 kJ��mol��1
C����43.5 kJ��mol��1 D����67.7 kJ��mol��1
����C
��������������ɵ������Ȼ�ѧ����ʽ��HCN(aq)��OH��(aq)===CN��(aq)��H2O(l)����H����12.1 kJ��mol��1��H��(aq)��OH��(aq)===H2O(l)����H����55.6 kJ��mol��1�����ݸ�˹���ɵõ���HCN(aq)===H��(aq)��CN��(aq)
��H��(��12.1 kJ��mol��1)��(��55.6 kJ��mol��1)����43.5 kJ��mol��1��
5��[2012���������ۣ�26(1)]��֪��ӦA��4HCl��O2CuO/CuCl2400 ��2Cl2��2H2O
��.��ӦA�У� 4 mol HCl���������ų�115.6 kJ��������
��.

��H2O�ĵ���ʽ��____________��
����ӦA���Ȼ�ѧ����ʽ��____________________________��
���Ͽ�1 mol H��O ����Ͽ� 1 mol H��Cl �������������ԼΪ________kJ��H2O��H��O ����HCl��H��Cl��(����ǿ����������)________��
������H�a�aH����4HCl(g)��O2(g)2Cl2(g)��2H2O(g)����H����115.6 kJ��mol��1
��32��ǿ
��������H2OΪ���ۻ���������ʽΪH�a�aH��������4 mol HCl�������ų�115.6 kJ���������ֽ�Ϸ�Ӧ����Ϊ400 ���������Ȼ�ѧ����ʽΪ4HCl(g)��O2(g)2Cl2(g)��2H2O(g)����H����115.6 kJ��mol��1�������������Ȼ�ѧ��Ӧ����ʽ��O2��Cl2�ļ��ܿ�֪������4 mol H��Cl����1 mol O===O�������յ�����������2 mol Cl��Cl����4 mol H��O���ų���������115.6 kJ����4 mol H��O���ļ��ܱ�4 mol H��Cl���ļ��ܴ�115.6 kJ��498 kJ��2��243 kJ��127.6 kJ���ʶϿ�1 mol H��O����Ͽ�1 mol H��Cl�������������ԼΪ127.6 kJ��4��32 kJ������H��O�����ܴ���H��Cl�����ܿ�֪��H��O����H��Cl��ǿ��
6��[2011���Ĵ����ۣ�29(1)]��֪1 g FeS2��ȫȼ�շų�7.1 kJ������FeS2ȼ�շ�Ӧ���Ȼ�ѧ����ʽΪ______________________________________��
����4FeS2(s)��11O2(g)===8SO2(g)��2Fe2O3(s)����H����3 408 kJ��mol��1
����������1 g FeS2��ȫȼ�շų�7.1 kJ�������������1 mol FeS2��ȫȼ�շų�������Ϊ852 kJ����÷�Ӧ���Ȼ�ѧ����ʽΪ4FeS2(s)��11O2(g)===8SO2(g)��2Fe2O3(s)����H����3 408 kJ��mol��1��
7��[2012���㶫���ۣ�31(4)]��Ҳ����������������Դ����﮵��صIJ��ϡ�
�õ�ط�ӦΪ2Li(s)��I2(s)===2LiI(s)����H
��֪��4Li(s)��O2(g)===2Li2O(s)����H1
4LiI(s)��O2(g)===2I2(s)��2Li2O(s)����H2
���ط�Ӧ����H��__________����缫��Ϊ�õ�ص�________����
����(��H1����H2)����
��������֪����4Li(s)��O2(g)===2Li2O(s)����H1
��4LiI(s)��O2(g)===2I2(s)��2Li2O(s)����H2
�ݸ�˹��������(������)�ɵ���2Li(s)��I2(s)===2LiI(s) ��H��(��H1����H2)��
�ɵ�ط�Ӧ��֪��I2�õ��ӱ���ԭ�����缫��Ϊ�õ�ص�������
8��[2011��ɽ����28(2)]��֪��2SO2(g)��O2(g)=2SO3(g) ��H����196.6 kJ��mol��1
2NO(g)��O2(g)=2NO2(g)����H����113.0 kJ��mol��1
��ӦNO2(g)��SO2(g)���SO3(g)��NO(g)����H��______kJ��mol��1��
������41.8
��������������������Ӧ����ʽ�ֱ��עΪ2SO2(g)��O2(g)���2SO3(g)����H1����196.6 kJ��mol��1��2NO(g)��O2(g)���2NO2(g)����H2����113.0 kJ��mol��1�������ܷ�Ӧ����ʽ����HΪ��H3����H3��������41.8 kJ��mol��1��
���̺�ǡ�
����һ����Ӧ�ȴ�С�ıȽϺͼ���
1�����и����Ȼ�ѧ����ʽ�У���ѧ��Ӧ����Hǰ�ߴ��ں��ߵ��� (����)
��C(s)��O2(g)===CO2(g)����H1
C(s)��O2(g)===CO(g)����H2
��S(s)��O2(g)===SO2(g)����H3
S(g)��O2(g)===SO2(g)����H4
��H2(g)��O2(g)===H2O(l)����H5
2H2(g)��O2(g)===2H2O(l)����H6
��CaCO3(s)===CaO(s)��CO2(g)����H7
CaO(s)��H2O(l)===Ca(OH)2(s)����H8
A���� B���� C���ڢۢ� D���٢ڢ�
����C
������������Ҫ���������H�������⣬��ȷ����H����������������������������ֵ��С��̼��������Ӧ���ȣ�����H1<0����H2<0��CO����O2����ʱ�ַ��ȣ�������H1<��H2�������Ĺ�̬���Ϊ��̬������ʱ����������������O2���ò���ͬ�����SO2ʱ����̬��ų��������࣬����H3>��H4������ͬ����ȼ�շ�Ӧ�����ʵ���Խ�࣬�ų�������Խ�࣬����H5>��H6��̼��Ʒֽ�������������H7>0��CaO��H2O��Ӧ�ų���������H8<0����Ȼ��H7>��H8���ʱ����ΪC��
2����������������Ӧ����1 molˮ��������241.8 kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ��__________����1 gˮ����ת����Һ̬ˮ����2.444 kJ����Ӧ2H2(g)��O2(g)===2H2O(l)����H��______kJ��mol��1��������ȼ����Ϊ_____kJ��mol��1��
����H2(g)��O2(g)===H2O(g)����H����241.8 kJ��mol��1����571.6��285.8
��������д�Ȼ�ѧ����ʽʱע�⣺��ѧ�������ı�ʱ����HҲͬ�ȱ����ĸı䣬������ˮ�������Ȼ�ѧ����ʽ��д�ɣ�H2(g)��O2(g)===H2O(g)����H����241.8 kJ��mol��1��2H2(g)��O2(g)===2H2O(g)����H����483.6 kJ��mol��1�ȶ�����ʽ��36 g��ˮ�������36 gҺ̬ˮʱ����36 g��2.444 kJ��g��1��88 kJ������2 mol H2ȼ������2 mol H2O(l)ʱ����H����483.6 kJ��mol��1��88 kJ��mol��1����571.6 kJ��mol��1��������ȼ����Ϊ1 mol H2ȼ������1 mol H2O(l)ʱ�ų�����������H��������285.8 kJ��mol��1��
���������˹���ɵ�Ӧ��
3����֪�����Ȼ�ѧ����ʽ
Fe2O3(s)��3CO(g)===2Fe(s)��3CO2(g)
��H1����25 kJ��mol��1 ��
3Fe2O3(s)��CO(g)===2Fe3O4(s)��CO2(g)
��H2����47 kJ��mol��1 ��
Fe3O4(s)��CO(g)===3FeO(s)��CO2(g)
��H3����19 kJ��mol��1 ��
д��FeO(s)��CO��ԭ��Fe��CO2���Ȼ�ѧ����ʽ________________��
����FeO(s)��CO(g)===Fe(s)��CO2(g) ��H����11 kJ��mol��1
���������ݸ�˹���ɣ���ѧ��Ӧ������һ����ɻ��Ƿּ�����ɣ��䷴Ӧ������ͬ�ġ�FeO��CO��Ӧ����ʽ��FeO(s)��CO(g)===Fe(s)��CO2(g)��ͨ���۲���Է��֣��˷�Ӧ���������������Ӧ����ʾ����[3������(2��������)]���ɵø÷�Ӧ�ķ�Ӧ�ȣ���H��[3��H1��(2��H3����H2)]����[3��(��25 kJ��mol��1)��(19 kJ��mol��1��2��47 kJ��mol��1)]����11 kJ��mol��1��
4����֪H2SO4(aq)��Ba(OH)2(aq)��Ӧ����H����1 584.2 kJ��mol��1��HCl(aq)��NaOH(aq)��Ӧ����H����55.6 kJ��mol��1��������BaSO4(s)�ķ�Ӧ�ȵ��� (����)
A����1 528.6 kJ��mol��1 B����1 473 kJ��mol��1
C����1 473 kJ��mol��1 D����1 528.6 kJ��mol��1
����B
������H��(aq)��OH��(aq)===H2O(l) ��H1����55.6 kJ��mol��1 ��
Ba2��(aq)��SO(aq)===BaSO4(s)����H2 ��
2H��(aq)��2OH��(aq)��Ba2��(aq)��SO(aq)===BaSO4(s)��2H2O(l)����H3����1 584.2 kJ��mol��1 ��
���ݸ�˹����֪����H3��2��H1����H2����H2����1 473 kJ��mol��1��
����ȴ�������
��һƪ���ڰ˵�Ԫ ��ѧ��Ӧ��������1��
��һƪ���ڰ˵�Ԫ ��ѧ��Ӧ��������3��
