化学实验复习
——气体的实验室制备、净化和收集
2016-01-08 15:15:53 来源:教师发展中心 撰稿:韩树团 摄影摄像: ; 评论:0 点击:
——气体的实验室制备、净化和收集
【考纲要求】
掌握常见气体实验室制法,包括所用试剂、仪器、反应原理和收集方法。
【复习内容】
1.气体的发生装置 ;
2.气体的净化干燥 ;
3.气体的收集 ;
4.尾气的处理 。
【模块一】1.气体的发生装置
【例题1】某兴趣小组利用SO2和O2在催化剂V2O5的作用下制备SO3固体,其过程中需要制备O2和SO2。
可供选用的装置有:
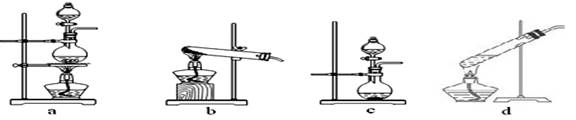
可供选用的药品有:
① 30%H2O ②MnO2 ③KClO3固体
④Na2SO3 ⑤铜片 ⑥浓硫酸
从下列图中选择适当仪器及药品,制备O2和SO2 ,用编号填写下表(有几种制法就填几种,不一定填满)
|
制取氧气 |
制取二氧化硫 |
||
|
装置编号 |
药品编号 |
装置编号 |
药品编号 |
|
c |
1.2 |
c |
4.6 |
|
b |
2.3 |
a |
5.6 |
|
d |
5.6 |
||
【知识归纳】
1.气体的发生装置
装置依据:所用药品的状态和反应条件。
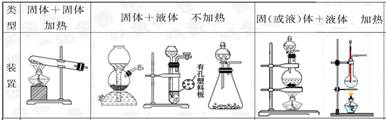
【例题2】制取下列气体分别可以使用那些装置?
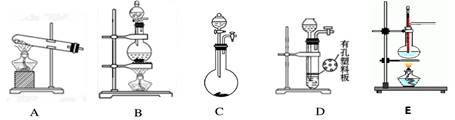
|
气体 |
氢气 |
氧气 |
二氧化碳 |
氯气 |
氨气 |
乙烯 |
乙炔 |
|
装置 |
CD |
AC |
CD |
B |
AC |
E |
C |
【模块二】2.气体的净化干燥
【回归教材】选修5
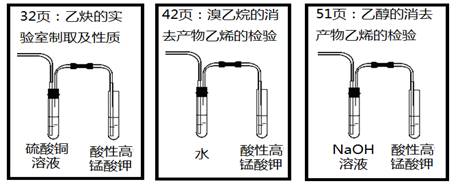
【思考交流】三套装置中:硫酸铜溶液、水、氢氧化钠溶液分别起什么作用?
【知识归纳】2.气体的净化干燥
(1)除杂试剂的选择依据:主要气体和杂质气体性质上的差异,如溶解性、酸碱性、
氧化性、还原性、可燃性等。
(2)除杂原则:
①不损失主要气体;
②不引入杂质气体。

【例题3】为下列各组气体选择合适的试剂(括号内为杂质气体)。
O2(Cl2)氢氧化钠溶液 Cl2(HCl)饱和食盐水
CO(CO2 )氢氧化钠溶液 NO( NO2)水
CO2( SO2 )酸性高锰酸钾 HCl(Cl2)四氯化碳
N2(O2)灼热的铜
【例题4】为了制备干燥、纯净的CO2,将大理石和盐酸反应生成的气体先后通过装有下列物质的两个吸收装置,两个装置中反应依次装入( A )。
①饱和NaHCO3溶液;无水CaCl2固体
②饱和NaHCO3溶液;浓硫酸
③浓硫酸;饱和NaHCO3溶液
④饱和Na2CO3溶液;稀硫酸
A.①② B.③④ C.①③ D.②④
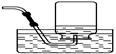
【例题5】如图实验室制备纯净的氯气,请回答下了问题。
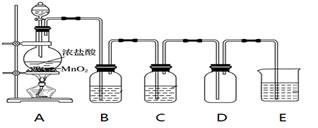
1)写出装置A中发生的反应方程式:MnO2+4HCl (浓)=MnCl2+Cl2↑+2H2O
2)装置B中装饱和食盐水试剂,作用是:除去氯气中的HCl
3)装置C中装浓硫酸试剂,作用是:除去氯气中的水
4)装置D采用的是什么样的收集方法:向上排空气法
【模块三】3.气体的收集
【知识归纳】
3.气体的收集
收集依据:气体的溶解性和密度。
|
排水法 |
向上排空气法 |
向下排空气法 |
|
难溶于水或微溶于水,又不与水反应的气体 |
密度大于空气 |
密度小于空气 |
|
|
|
|
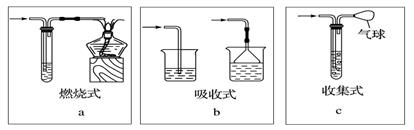
【例题6】用如图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是( C )
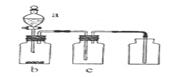
|
气体 |
a |
b |
c |
|
|
A |
NO2 |
浓硝酸 |
铜片 |
NaOH溶液 |
|
B |
SO2 |
浓硫酸 |
铜片 |
酸性KMnO4溶液 |
|
C |
CO2 |
稀硫酸 |
Na2C O3固体 |
浓硫酸 |
|
D |
NH3 |
浓氨水 |
生石灰 |
浓硫酸 |
【例题7】用下图所示装置制取表中的四种干燥、纯净的气体(图中加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。( D )

|
气体 |
a |
b |
c |
d |
|
|
A |
CO2 |
稀盐酸 |
CaCO3 |
饱和Na2CO3 |
浓H2SO4 |
|
B |
Cl2 |
浓盐酸 |
MnO2 |
NaOH溶液 |
浓H2SO4 |
|
C |
SO2 |
稀H2SO4 |
Cu |
品红溶液 |
浓H2SO4 |
|
D |
O2 |
H2O2 |
MnO2 |
浓H2SO4 |
浓H2SO4 |
上述方法中可以得到干燥、纯净的气体是
A.CO2 B.Cl2 C.SO2 D.O2
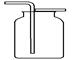
【例题8】实验室可用下图所示装置干燥、收集某气体R,并吸收多余的R,则R是 ( D )
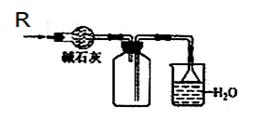
A.O2 B.HCl C.Cl2 D.NH3
【模块四】4.尾气的处理
【知识归纳】
4.尾气的处理
吸收依据:气体的性质。
【小结】实验室气体制备的基本流程
反应原理---- 制备装置--------净化干燥--------气体收集---------尾气吸收
【链接高考、练出高分】
1、(10年重庆理综·8)下列实验装置图正确的是(B )

2.水蒸气通过的灼热的焦炭后,流出气体的主要成分是CO是H2,还有CO2和水蒸气等。请用下图中提供的仪器,选择必要的试剂,设计一个实验,证明上述混合气体中有CO和H2。(加热装置和导管等在图中略去)
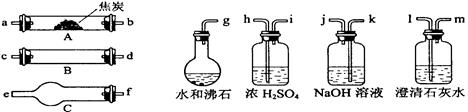
回答下列问题:
(1)盛浓H2SO4的装置用途是 ,盛NaOH溶液的装置用途是 。
(2)仪器B中需加入试剂的名称(或化学式)是: ,
所发生反应的化学方程是: ,
(3)仪器C中需加入试剂的名称(或化学式)是: ,
其目的是 。
(4)按气流方向连接各仪器,用字母表示接口的连接顺序:
g—ab— 。
(5)能证明混合气中含有CO的实验依据是 。
(6)能证明混合气中含有H2的实验依据是
3.在呼吸面具和潜水艇中可用过氧化钠作为供养剂。请选择适当的化学试剂和实验用品,用下图中的实验装置进行试验,证明过氧化钠可作供养剂。
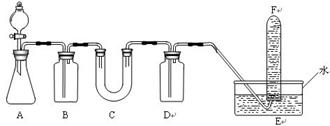
(1)A是制取CO2的装置。写出A中发生反应的化学方程式:
__________________________________
(2)填写表中空格:
(3)写出过氧化钠与二氧化碳反应的化学方程式:_________________。
(4)试管F中收集满气体后,下一步实验操作是:
4.某化学兴趣小组为探究在实验室制备较为纯净N2的方法,进行了认真的准备。
【查阅资料】N2的制法有下列三种方案:
方案1:加热NaNO2和NH4Cl的浓溶液制得N2。
方案2:加热条件下,以NH3还原CuO可制得N2,同时获得活性铜粉。
方案3:将空气缓缓通过灼热的铜粉获得较纯的N2。
【实验准备】以实验室常见仪器(药品)等设计的部分装置如下图(加热仪器未画出)。
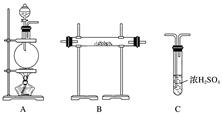
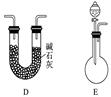
【分析交流】
(1)若以方案1制得N2,应选择的发生装置是_______。
(2)若按方案2制得干燥、纯净的N2,且需要的NH3以生石灰和浓氨水作原料,整套制气装置按气流从左到右的连接顺序是__________(填序号)。获得N2的反应原理是___________________________________(写反应方程式)。
(3)若以排水法收集N2,其中会混入水蒸气。但也不宜用排空气法,其原因是___________________________________。你提出的收集方法是______。
5.某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
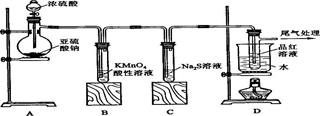
请到答F列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是 ,其中发生反应的化学方程式为 ;
(2)实验过程中,装置B、C中发生的现象分别是 、
,这些现象分别说明SO2具有的性质是 和 ;装置B中发生反应的离子方程式为 ;
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象 ;
(4)尾气可采用 溶液吸收。
6.(12年山东理综·30)(4)实验室制备H2和Cl2通常采用下列反应:
Zn+H2SO4=ZnSO4+H2↑
MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
据此,从下列所给仪器装置中选择制备并收集H2的装置 (填代号)和制备并收集干燥、纯净Cl2的装置 (填代号)。可选用制备气体的装置:
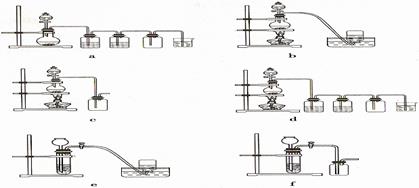
相关热词搜索:
上一篇:第二节 水的电离和溶液的酸碱性
下一篇:《有趣的语言翻译》教学设计