第十三单元 化学实验
2015-12-01 08:36:55 来源: 撰稿:董啸 摄影摄像: ; 评论:0 点击:
第十三单元 化学实验
|
|
|
授课人:董 啸 |
|
|
①了解一般事故处理方法,能对常见物质进行检验、分离和提纯。
|
|
|
教学目标: |
②了解实验室常用仪器的主要用途和用法,能根据要求配制溶液。
|
|
|
|
③掌握化学实验的基本操作,掌握常见气体的实验室制法。 |
|
|
教学重点: |
物质的制备、检验、分离提纯 |
|
|
教学难点: |
设计、评价或改进实验方案 |
|
|
教学方法: |
讲练结合 |
|
|
教学过程: |
|
|
典型试题剖析
一、高考新题赏析
1、(2012新课标)7.下列叙述中正确的是【A】
A.液溴易挥发,在存放液溴的试剂瓶中应加水封
B.能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2
C.某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I-
D.某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+
2、(2012浙江卷)8.下列说法正确的是
A.在“镀锌铁皮的镀层厚度的测定”实验中,将镀锌铁皮放入稀硫酸,待产生氢气的速率突然减小,可以判断锌镀层已反应完全
B.在“火柴头中氯元素的检验”实验中,摘下几根未燃过的火柴头,将其浸于水中,稍后取少量溶液于试管中,滴加硝酸银溶液和稀硝酸后,即可判断氯元素的存在
C.在“硫酸亚铁铵的制备”实验中,为了得到硫酸亚铁铵晶体,应小火加热蒸发皿,直到有大量晶体析出时停止加热
D.受强酸或强碱腐蚀致伤时,应先用大量水冲洗,再用2%醋酸溶液或饱和硼酸溶液洗,最后用水冲洗,并视情况作进一步处理
3、(2012江苏高考)6. 用下列实验装置进行相应实验,能达到实验目的的是
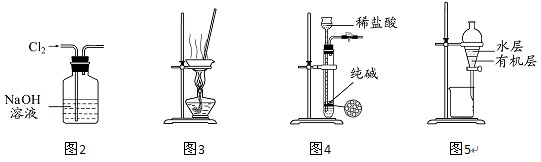
A. 用图2 所示装置除去Cl2中含有的少量HCl
B. 用图3 所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C. 用图4 所示装置制取少量纯净的CO2气体
D. 用图5 所示装置分离CCl4萃取碘水后已分层的有机层和水层
2、(2012江苏高考)13. 下列根据实验操作和现象所得出的结论正确的是
|
选项 |
实验操作 |
实验现象 |
结论 |
|
A |
向两份蛋白质溶液中分别滴加饱和NaCl 溶液和CuSO4 溶液 |
均有固体析出 |
蛋白质均发生变性 |
|
B |
向溶液X 中先滴加稀硝酸,再滴加Ba(NO3)2溶液 |
出现白色沉淀 |
溶液X 中一定含有SO42- |
|
C |
向一定浓度的Na2SiO3 溶液中通入适量CO2 气体 |
出现白色沉淀 |
H2SiO3 的酸性比H2CO3的酸性强 |
|
D |
向浓度均为0. 1 mol·L-1 NaCl 和NaI 混合溶液中滴加少量AgNO3 溶液 |
出现黄色沉淀 |
Ksp(AgCl)>Ksp(AgI) |
2、(2012安徽高考)10.仅用下表提供的玻璃仪器(非玻璃仪器任选)就能实现相应实验目的的是
|
选项 |
实验目的 |
玻璃仪器 |
|
A |
分离乙醇和乙酸乙酯的混合物 |
分液漏斗、烧杯 |
|
B |
用PH=1的盐酸配置100mL PH=2的盐酸 |
100mL容量瓶、烧杯、玻璃棒、胶头滴管 |
|
C |
用溴水、淀粉-KI溶液比较Br2与I2的氧化性强弱 |
试管、胶头滴管 |
|
D |
用NH4Cl固体和Ca(OH)2固体制备并收集NH3 |
酒精灯、烧杯、导管、集气瓶 |
3、(2012年北京高考)8.下列试验中,所选装置不合理的是
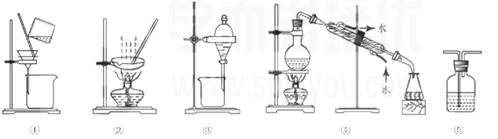
A. 分离Na2CO3溶液和CH3COOC2H5,选④
B. 用CC14提取碘水中的碘,选③
C. 用FeC12,溶液吸收C12选⑤
D. 粗盐提纯,选①和②
4、(2012天津卷)4.完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是 ( )
|
|
A |
B |
C |
D |
|
实 验 |
用CCl4提取 溴水中的Br2 |
除去乙醇中的苯酚 |
从KI和I2的固体 混合物中回收I2 |
配制100 mL 0.1000 mol·L-1 K2Cr2O7溶液 |
|
装 置 或 仪 器 |
|
|
|
|
5、(2012年北京高考)10.用右图所示装置进行下列实验,实验结果与预测的现象不一致的是


3、(2012重庆卷)8.对实验:①中和滴定、②中和热的测定、③实验室制备乙烯、④乙酸乙酯的制取,叙述正确的是
A.①④必须加热 B.②③必须隔热 C.①②必须用指示剂 D.③④必须用催化剂
6、(2012浙江卷)13.水溶液X中只可能溶有K+、Mg2+、Al3+、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的若干种离子。某同学对该溶液进行了如下实验:
中的若干种离子。某同学对该溶液进行了如下实验:

下列判断正确的是
A.气体甲一定是纯净物 B.沉淀甲是硅酸和硅酸镁的混合物
C.K+、![]() 和
和![]() 一定存在于溶液X中 D.
一定存在于溶液X中 D.![]() 和
和![]() 一定不存在于溶液X中
一定不存在于溶液X中
5、(2012新课标)28.(14分)
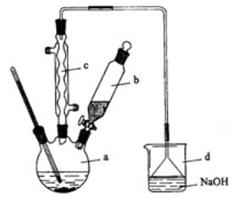
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
按下列合成步骤回答问题:
|
|
苯 |
溴 |
溴苯 |
|
密度/g·cm-3 |
0.88 |
3.10 |
1.50 |
|
沸点/°C |
80 |
59 |
156 |
|
水中溶解度 |
微溶 |
微溶 |
微溶 |
(1)在a中加入15mL无水苯和少量铁屑。在b中小心加入4.0mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了___气体。继续滴加至液溴滴完。装置d的作用是____;
答案:HBr; 吸收HBr和Br2
(2)液溴滴完后,经过下列步骤分离提纯:
1向a中加入10mL水,然后过滤除去未反应的铁屑;
2滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是_____
3向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是_____;
答案:2除去HBr和未反应的Br2;3干燥
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为___,要进一步提纯,下列操作中必须的是____(填入正确选项前的字母);
答案:苯;【C】
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是___(填入正确选项前的字母)。【B】
A.25mL B.50mL C.250mL D.500mL
9、(2012浙江卷)28.[14分]实验室制备苯乙酮的化学方程式为:

制备过程中还有![]() 等副反应。
等副反应。
主要实验装置和步骤如下:


(I)合成:在三颈瓶中加入20 g无水AlCl3和30 mL无水苯。为避免反应液升温过快,边搅拌边慢慢滴加6 mL乙酸酐和10 mL无水苯的混合液,控制滴加速率,使反应液缓缓回流。滴加完毕后加热回流1小时。
(Ⅱ)分离与提纯:
①边搅拌边慢慢滴加一定量浓盐酸与冰水混合液,分离得到有机层
②水层用苯萃取,分液
③将①②所得有机层合并,洗涤、干燥、蒸去苯,得到苯乙酮粗产品
④蒸馏粗产品得到苯乙酮。回答下列问题:
(1)仪器a的名称:____________;装置b的作用:________________________________。
(2)合成过程中要求无水操作,理由是____________________________________________。
(3)若将乙酸酐和苯的混合液一次性倒入三颈瓶,可能导致_________________。
A.反应太剧烈 B.液体太多搅不动 C.反应变缓慢 D.副产物增多
(4)分离和提纯操作②的目的是_____________________________________________________。该操作中是否可改用乙醇萃取?_____(填“是”或“否”),原因是_________________。
(5)分液漏斗使用前须___________________并洗净备用。萃取时,先后加入待萃取液和萃取剂,经振摇并______________________后,将分液漏斗置于铁架台的铁圈上静置片刻,分层。分离上下层液体时,应先__________,然后打开活塞放出下层液体,上层液体从上口倒出。
(6)粗产品蒸馏提纯时,下来装置中温度计位置正确的是________________,可能会导致收集到的产品中混有低沸点杂质的装置是________________。


答案:28.[15分]
(1)干燥管; 吸收HCl气体。
(2)防止三氯化铝和乙酸酐水解(只答三氯化铝水解或乙酸酐水解也可)
(3)AD;
(4)把溶解在水中的苯乙酮提取出来以减少损失; 否, 乙醇与水混溶。
(5)检漏; 放气; 打开上口玻璃塞;(或使塞上的凹槽对准漏斗上口的小孔);
(6)C; AB。
9、(2012全国卷)28.(15分)(注意:在试题卷上作答无效)
现拟用下图所示装置(尾气处理部分略)来制取一氧化碳,并用以测定某铜粉样品(混有CuO粉末)中金属铜的含量。
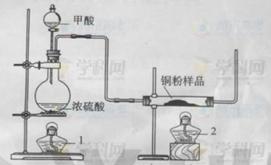
(1)制备一氧化碳的化学方程式是 HCOOH=CO+H2O ;
(2)试验中,观察到反应管中发生的现象时黑色粉末变红 ;
尾气的主要成分是 CO、CO2 ;
(3)反应完成后,正确操作顺序为 c b a (填字母)
a.关闭漏斗开关 b.熄灭酒精1 c.熄灭酒精灯2
(4)若试验中称取铜粉样品5.0g,充分反应后,反应管中剩余固体的质量为4.8g,则原样品中单质铜的质量分数为 0.96 ;
(5)从浓硫酸、浓硝酸、蒸馏水、双氧水中选用合适的试剂,设计一个测定样品中金属铜质量分数的方案;
①设计方案的主要步骤是(不必描述操作过程的细节) 将浓硫酸用蒸馏水稀释,将样品与稀硫酸充分反应后过滤、干燥、称量剩余固体铜的质量 ;
②写出有关反映的化学方程式 CuO+H2SO4= CuSO4+H2O 。
10、(2012重庆卷)27.(15分)氯离子插层镁铝水滑石![]() 是以中国新型离子交换材料,其在高温下完全分解为
是以中国新型离子交换材料,其在高温下完全分解为![]() 和水蒸气,现用题27图装置进行试验确定其化学式(固定装置略去)。
和水蒸气,现用题27图装置进行试验确定其化学式(固定装置略去)。

(1)![]() 热分解的化学方程式为 。
热分解的化学方程式为 。
(2)若只通过测定装置C、D的增重来确定![]() ,则装置的连接顺序为 (按气流方向,用接口字母表示),其中C的作用是 。装置连接后,首先要进行的操作名称是 。
,则装置的连接顺序为 (按气流方向,用接口字母表示),其中C的作用是 。装置连接后,首先要进行的操作名称是 。
(3)加热前先通过![]() 排尽装置中的空气,称取C、D的初始质量后,再持续通入
排尽装置中的空气,称取C、D的初始质量后,再持续通入![]() 的作用是 、 等.
的作用是 、 等.
(4)完全分解后测得C增重3.65g 、D增重9.90g ,则![]() = .若取消冷却玻管B后进行试验,测定
= .若取消冷却玻管B后进行试验,测定![]() 值将 (填“偏高”或“偏低”)
值将 (填“偏高”或“偏低”)
(5)上述水滑石在空气中放置时易发生反应生成,该生成物能发生类似的热分解反应,现以此物为样品,用(2)中连接的装置和试剂进行试验测定![]() ,除测定D的增重外,至少还需测定 .
,除测定D的增重外,至少还需测定 .

答案:

二、经典试题回顾
〖板书设计〗
〖教后记〗
相关热词搜索:
上一篇:第十三单元 化学实验(5)
下一篇:最后一页