��ʮһ��Ԫ ˮ��Һ�е�����ƽ�⣨4��
2015-11-25 09:51:29 ��Դ�� �壺��Х ��Ӱ���� ; ���ۣ�0 �����
��ʮһ��Ԫ ˮ��Һ�е�����ƽ�⣨4��
|
|
|
�ڿ��ˣ��� Х |
|
|
������ԭ����ƽ��ԭ��������ˮ���ԭ���� |
|
|
��ѧĿ�꣺ |
��������ҺpH��������Ũ�ȡ�����������Ũ�ȵļ��㣻 |
|
|
|
������ƽ���ƶ�ԭ������ijЩ���⡣
|
|
|
��ѧ�ص㣺 |
ҺpH��������Ũ�ȡ�����������Ũ�ȵļ��� |
|
|
��ѧ�ѵ㣺 |
����ƽ���ƶ�ԭ������ijЩ���� |
|
|
��ѧ������ |
���������������Ƚϣ����ֹ��� |
|
|
��ѧ���̣� |
���Ŀ�ʱ |
|
����֪ʶ����
�ġ��ε�ˮ��
1���ε�ˮ��
��1�����壺�ε������ijһ�ֻ�������Ӹ�ˮ���������H����OH-�������������ʵķ�Ӧ���������ˮ�⡣
�ζ�Ӧ����(���)Խ����ˮ��̶�Խ����Һ����(������)Խǿ�����������ˮ��ij̶�һ���С�����������ˮ�ⷽ��ʽ��һ���ÿ��淴Ӧ���ţ�������������������������ˮ��ķ���ʽҪ�ֲ�д��
��2��ˮ��ʵ�ʣ�
�ε����������ʹˮ�ĵ���ƽ�ⷢ���ƶ����Ӷ�ʹ��Һ�����Ի���ԡ�
��3��ˮ����ɣ�
������ˮ�⣬������ˮ�⣬Խ��Խˮ�⣬˭ǿ��˭�ԡ�
��4��ˮ�����ӷ���ʽ��ʾ������
��һ����˵������ˮ��ij̶Ȳ���Ӧ���ÿ���ű�ʾ������ˮ��һ�㲻��������������壬���Բ��÷�������������������ʾˮ����
��Cu2����2H2O�PCu(OH)2��2H����NH��H2O�PNH3��H2O��H����
����Ԫ�����ε�ˮ���Ƿֲ����еģ�ˮ�����ӷ���ʽҪ�ֲ���ʾ����Na2CO3ˮ�ⷴӦ�����ӷ���ʽΪ��CO��H2O�PHCO��OH����HCO��H2O�PH2CO3��OH����
����Ԫ���������ӵ�ˮ���һ����ɣ���FeCl3��Һ�У�Fe3����3H2O�PFe(OH)3��3H����
��˫ˮ��ֱ������Ժͼ��Ե�������������ٽ�ˮ��̶Ƚϴ���дʱҪ����===�������������������ȣ���NaHCO3��AlCl3�����Һ�ķ�Ӧ���ӷ���ʽ��Al3����3HCO===Al(OH)3����3CO2����
��Ҫ��ˮ�ⷴӦ����ʽ:
�Ȼ�泥�NH��H2O�PNH3��H2O��H��
�����ƣ�CH3COO����H2O�PCH3COOH��OH��
̼���ƣ�CO��H2O�PHCO��OH����HCO��H2O�PH2CO3��OH��
AlCl3��Һ��Al3����3H2O�PAl(OH)3��3H��
FeCl3��Һ��Fe3����3H2O�PFe(OH)3��3H��
NaHCO3��AlCl3�����Һ��Al3����3HCO===Al(OH)3����3CO2��
NaAlO2��AlCl3�����Һ��Al3����3 AlO2����6H2O ===4Al(OH)3��
��5������ˮ��Ĺ��ɼ���չӦ��
����˭��˭ˮ�⣬Խ��Խˮ�����������ԣ�HCN<CH3COOH������ͬ�����¼��ԣ�NaCN>CH3COONa��
��ǿ�����ʽ��ֻ���룬��ˮ�⣬��Һ�����ԡ���NaHSO4��ˮ��Һ�У�NaHSO4===Na����H����SO��
���������ʽ����Һ������ԣ�ȡ������ʽ������ӵĵ���̶Ⱥ�ˮ��̶ȵ���Դ�С��
������̶�С��ˮ��̶ȣ���Һ�ʼ��ԡ���NaHCO3��Һ�У�
HCO�PH����CO(��Ҫ)��HCO��H2O�PH2CO3��OH��(��Ҫ)��
������̶ȴ���ˮ��̶ȣ���Һ�����ԡ���NaHSO3��Һ�У�HSO�PH����SO(��Ҫ)��HSO��H2O�PH2SO3��OH��(��Ҫ)��
����ͬ�����µ�ˮ��̶ȣ�����>��Ӧ��ʽ�Σ���CO>HCO��
����ٽ�ˮ�����>����ˮ�����>ˮ������Ƶ��Ρ���NH��ˮ�⣺(NH4)2CO3>(NH4)2SO4>(NH4)2Fe(SO4)2��
����CH3COONH4��Һ�����ԣ���NH4HCO3��Һ�Լ��ԡ�
�����˼����
1����ʽ����Һһ����������
������һ������ʽ����Һ���������ԣ���NaHSO4��Һ��Ҳ�����Լ��ԣ���NaHCO3��Һ�ȡ�
2�����ʵ���Ũ����ͬ��������Һ�У������Ӻͷ������������� (����)
A��CaCl2 B��CH3COONa C����ˮ D��K2S
����D
������A������Ca2����Cl����H2O��H����OH����B������CH3COO����Na����H2O��CH3COOH��H����OH����C������NH3��NH3��H2O��H2O��H����OH����NH��D������K����S2����HS����H2O��H2S��H����OH����
3����������ķ�������NaCl��Һ���Ȼ����Һ��̼������Һ��
����������Һ��ȡ�����ֱ������ɫʯ����Һ������ɫ��ΪNaCl��Һ�����ɫ��Ϊ�Ȼ����Һ������ɫ��Ϊ̼������Һ��
4������֤��Na2CO3��Һ�ʼ�������COˮ������ģ�
�𰸡�����Һ�е����̪��Һ����Һ�Ժ�ɫ�����������Һ�е�������Ȼ�����Һ��������ɫ����������Һ�ĺ�ɫ��ȥ�������˵��������Һ�ʼ�������CO����ġ�
5��ͬŨ�ȵ�Na2CO3��CH3COONa��Һ��ȣ�˭��pH�ϴ�Ϊʲô��ͬŨ�ȵ�Na2CO3��NaHCO3����أ�
�𰸡�Na2CO3��Һ��pH����ΪCH3COOH������ǿ��H2CO3����CO���H��������ǿ��CH3COO������COˮ��̶Ƚϴ�����c(OH��)�ϴ�pH�ϴ������εĶ���ˮ�����һ��ˮ�⣬��Na2CO3��Һ��pH��NaHCO3��
6��д�������������ܷ���ˮ�ⷴӦ�����ӷ���ʽ��
�������������ơ���С�մ���ƫ�����ơ�����������
������Al3����3H2O�PAl(OH)3��3H�� ��S2����H2O�PHS����OH����HS����H2O�PH2S��OH�� ��HCO��H2O���PH2CO3��OH�� ��AlO��2H2O�PAl(OH)3��OH�� ����ˮ��
2��Ӱ�����أ�
������
����Խ�������Ӧ����������ӻ����������ӵ�ˮ��̶�Խ����Һ�ļ��Ի�����Խǿ��
������
|
���� |
ˮ��ƽ�� |
ˮ��̶� |
ˮ��������ӵ�Ũ�� |
|
|
�¶� |
���� |
���� |
���� |
���� |
|
Ũ�� |
���� |
���� |
��С |
���� |
|
��С(��ϡ��) |
���� |
���� |
��С |
|
|
������ |
�� |
���������ӵ�ˮ��̶���С |
||
|
�� |
��������ӵ�ˮ��̶���С |
|||
���ۣ�Խ��Խˮ�⣬Խ��Խˮ�⣬ԽϡԽˮ�⣬�������ƻ�ٽ�ˮ�⡣
��ע�⡿��
�� ϡ��Һ����Դٽ�ˮ�⣬ˮ��ƽ�����ơ�
�� H��������������ˮ�⣬�ٽ�������ˮ�⣻OH��������������ˮ�⣬�ٽ�������ˮ�⡣
����Ԫ���������������ӱ���ʽ�������ˮ��̶ȴ�ö࣬��Һ�ļ��Ը�ǿ��
��CH3COONH4 ��Һ�����ԣ� NH4F��Һ�����ԣ� NH4HCO3 ��Һ�Լ���.
�����˼����
1��ϡ��Һ�У��ε�Ũ��ԽС��ˮ��̶�Խ������Һ����(�����)ҲԽǿ��
��������Һ��Ũ��ԽС��ˮ��̶�Խ��������Һ������Ũ��С����Ҫ���أ�����Һ����(�����)Խ����
2��������Ϊ����CH3COONa��Һ�У��������������ᣬ����CH3COONa��Һˮ�������OH����Ӧ��ʹƽ����ˮ�ⷽ���ƶ�������˵������Ϊʲô��
�𰸡����ԣ�ԭ���ǣ���ϵ��c(CH3COOH)����������ˮ�⣬��ʹƽ��
CH3COO����H2O�PCH3COOH��OH�����ơ�
3��˫ˮ�⣺
�����Һ�е���������ͬʱˮ�⣬��ٽ���ʹ���εļ���ˮ����ȫ������˫ˮ��ʱ�����ˮ��ij̶Ƚϴ����������ˮ�ⷽ��ʽ��һ�㲻�ÿ��淴Ӧ����,����������������������
�������У�Al3+��HCO3-��CO32-��AlO2-��S2-��HS-��Fe3+��HCO3-��CO32-��AlO2-��NH4+�� CH3COO-Ҳ����˫ˮ�⣬���̶Ȳ���
�ر�������NH��CH3COO����HCO���ܷ���˫ˮ�ⷴӦ�����ܴ������档
4���ε�ˮ���Ӧ��
���ж���Һ����Լ����ʵļ���
���Ƚ�����Һ������Ũ�ȵĴ�С��
���ж������Ƿ棻
����Һ�����úʹ��档
������Һ��������ʱ���ò���ļ�������
a.һ�������Һˮ�������ѻӷ�����ʱ�����ɺ�һ���ԭ���ʡ���CuSO4(aq)CuSO4(s)��
b.����Һˮ�������ӷ�����ʱ���������պ�һ��ö�Ӧ���������AlCl3(aq)Al(OH)3Al2O3��
c.�����ȷֽ����������Ӧ�����������պ�һ��÷�Ӧ���
Ca(HCO3)2��NaHCO3��KMnO4��NH4Cl���������ֽ⣬����������պ�ֱ�ΪCa(HCO3)2�D��CaCO3(CaO)��NaHCO3�D��Na2CO3��NH4Cl�D��NH3����HCl����
��ԭ����������ʱ�ᱻO2���� ���磬Na2SO3(aq)Na2SO4(s)��
�ε�ˮ���Ӧ��:
|
Ӧ�� |
���� |
|
�ж���Һ������� |
FeCl3��Һ�����ԣ�ԭ����Fe3����3H2O�PFe(OH)3��3H�� |
|
�ж�����ǿ�� |
NaX��NaY��NaZ������pH�ֱ�Ϊ8��9��10��������HX>HY>HZ |
|
���ƻ�������ˮ�������Һ |
����CuSO4��Һʱ����������H2SO4����ֹCu2��ˮ�⣬����FeCl3��Һ�������������� |
|
�������ȡ |
��Fe(OH)3�������ӷ�Ӧ��Fe3����3H2OFe(OH)3(����)��3H�� |
|
���ʵ��ᴿ |
��ȥMgCl2��Һ�е�Fe3�����ɼ���MgO��þ�ۡ�Mg(OH)2��MgCO3 |
|
��ĭ�����ԭ�� |
�ɷ�ΪNaHCO3��Al2(SO4)3��������ӦΪ: Al3����3HCO===Al(OH)3����3CO2�� |
|
����ˮ�� |
����������ˮ����ԭ��ΪAl3����3H2O�PAl(OH)3(����)��3H�� |
|
���ʵ�ʹ�� |
�̬�������ľ�Ҳ��û��� |
![]() ���˼��
���˼��![]()
1������ϴ�����۵�ԭ����ʲô��Ϊʲô˵�ȵĴ�����Һȥ������ǿ��
����CO��H2O�PHCO��OH�������ȣ��ٽ�CO��ˮ�⣬��Һ������ǿ��ȥ
��������ǿ��
2��������ȥMgCl2��Һ��Fe3������ԭ����ʲô��
����MgCl2��Һ�л���������Fe3������ʱ���ɼ���Mg��MgO��Mg(OH)2��MgCO3����ȥFe3������ԭ����Fe3����ˮ��̶ȱ�Mg2����ˮ��̶ȴ�����Щ���ʣ�����Fe3����3H2O�PFe(OH)3��3H��ƽ�����ƣ�����Fe(OH)3������ȥ��
3�������ж���ʽ����Һ������ԣ��Ծ���˵����
������ʽ�ε�ˮ��Һ��ʲô���ʣ�Ҫ�����ε�������ӵ����ʡ�
(1)ǿ�����ʽ��ֻ���룬��ˮ�⣬һ�������ԡ�
��NaHSO4��NaHSO4===Na����H����SO��
(2)�������ʽ�δ����������ƣ��ȴ��ڵ���ƽ���ִ���ˮ��ƽ�⣺
HA���PH����A2��(���룬������)
HA����H2O�PH2A��OH��(ˮ�⣬�Լ���)
�������̶ȴ���ˮ��̶ȣ��������ԣ���H2PO��HSO�ȣ����ˮ��̶ȴ��ڵ���̶ȣ����Լ��ԣ���HCO��HS����HPO�ȡ�
5������Һ�е������غ�
������غ�:
�������Һ�У����۴��ڶ��������ӣ�����Һ���dzʵ����ԣ����������������������һ���������������������������������غ���ɡ�
NH4Cl��Һ�д��ڣ�c(NH4+)+ c(H+)= c(Cl-) +c(OH-)��
CH3COONa��Һ�д��ڣ�c(H+) + c(Na+)= c(CH3COO-) +c(OH-)��
Na2CO3��Һ�д�����c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-)��
NaHCO3��Һ�д�����c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-)��
Ӧ�ã�
a. c(NH4+) > c(Cl-)>c(H+)>c(OH-) (��)
b.��c(NH4+)��c(Cl-)��������Ͱ�ˮ�Ļ����Һ�����ԡ�
��c(NH4+)> c(Cl-)��������Ͱ�ˮ�Ļ����Һ�ʼ��ԡ�
��c(NH4+)��c(Cl-)��������Ͱ�ˮ�Ļ����Һ�����ԡ�
�������غ㣺
�������Һ�У�����ijЩ�����ܹ�ˮ�⣬�����������࣬��ԭ�������غ�ģ����������غ����������غ���ɡ�
NH4Cl��Һ�д�����c(Cl-)= c(NH4+)+c(NH3��H2O)
CH3COONa��Һ�д��ڣ�c(Na+)= c(CH3COO-) +c(CH3COOH)
Na2CO3��Һ�д�����c(Na+)/2=c(CO32-)+c(HCO3-)+c(H2CO3) ��
c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3) ]
NaHCO3��Һ�д�����c(Na+)= c(CO32-)+c(HCO3-)+c(H2CO3)
�������غ㣺
������Һ�У���ˮ�������������Ũ�ȵ�����ˮ�����������������Ũ�ȣ�����ǿ����������˵����Һ�е�����������Ũ�ȵ���ˮ�����ĵ������Ӻ�ʣ��������Ũ��֮�͡�
NH4Cl��Һ�д�����c(H+)= c(OH-)+c(NH3��H2O)
CH3COONa��Һ�д��ڣ�c(OH-)= c(H+)+c(CH3COOH)��
Na2CO3��Һ�д��ڣ� c(OH-) =c(HCO3��)+ c(H+)��2c(H2CO3)
NaHCO3��Һ�д����� c(OH-) =c(H2CO3)+ c(H+)��c(CO32-)
˵���������غ�����ɵ���غ�������غ��Ƴ���
��֪ʶ��չ��Na2CO3��NaHCO3�����Һ�е������غ�
��1��Na2CO3��NaHCO3��1��1�����Һ
������غ㣺c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-)
�������غ㣺c(Na+)��2/3=c(CO32-)+c(HCO3-)+c(H2CO3)
�������غ㣺
�ɢٺ͢ڿ����Ƴ���2c(OH-)= c(HCO3-)+3c(H2CO3)+2c(H+)��c(CO32-)
��2��Na2CO3��NaHCO3��2��1�����Һ
������غ㣺c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-)
�������غ㣺c(Na+)��3/5=c(CO32-)+c(HCO3-)+c(H2CO3)
�������غ㣺
�ɢٺ͢ڿ����Ƴ���3c(OH-)= 2c(HCO3-)+5c(H2CO3)+3c(H+)��c(CO32-)
��3��Na2CO3��NaHCO3��1��2�����Һ
������غ㣺c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-)
�������غ㣺c(Na+)��3/4=c(CO32-)+c(HCO3-)+c(H2CO3)
�������غ㣺
�ɢٺ͢ڿ����Ƴ���3c(OH-)= c(HCO3-)+4c(H2CO3)+3c(H+)��2c(CO32-)
6������Ũ�ȴ�С�Ƚϣ�
(1)��Ԫ����(H2A)��Һ:c(H+)>c(HA-)>c(A2-)>c(OH-)��
(2)��ͬ��Һ��ͬһ����Ũ�ȵıȽϣ�Ҫ����Һ���������Ӷ���Ӱ������ء�������ͬ�����ʵ���Ũ�ȵ�������Һ�У���NH4C1����CH3COONH4����NH4HSO4��c(NH4+)�ɴ�С��˳������>��>����
(3)����������Ũ�ȵıȽ�����
��0.1mol/LNH4Cl��Һ��
c(Cl-)>c(NH4+)>c(H+)>c(OH-)��c(H+)+c(NH4+)= c(Cl-)+c(OH-)
��0.1mol/LCH3COONa��Һ��
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)��c(H+) + c(Na+)= c(CH3COO-) +c(OH-)
��0.1mol/LHCl��0.1mol/LNH3��H2O��Һ����������
c(Cl-)>c(NH4+)>c(H+)>c(OH-)��
��0.1mol/LNaOH��0.1mol/LCH3COOH��Һ����������
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)��
��0.1mol/LHCl��0.2mol/LNH3��H2O��Һ����������
c(NH4+) > c(Cl-) > c(OH-)> c(H+)��
pH=2�����pH=12��ˮ�������ϣ�
c(NH4+) > c(Cl-) > c(OH-)> c(H+)
��0.1mol/LNaOH��0.2mol/LCH3COOH��Һ����������
c(CH3COO-)>c(Na+)>c(H+) > c(OH-)��
pH=2�����pH=12NaOH��Һ�������ϣ�
c(CH3COO-)>c(Na+)>c(H+) > c(OH-)
��0.2mol/LHCl��0.1mol/LNH3��H2O��Һ����������
c(Cl-) > c(H+)>c(NH4+)> c(OH-)
��0.2mol/LNaOH��0.1mol/LCH3COOH��Һ����������
c(Na+) > c(OH-)> c(CH3COO-)> c(H+)
��0.1mol/L NaHCO3��Һ��
c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(H2CO3)>c(CO32-)
��0.1mol/L Na2CO3��Һ��
c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H2CO3)>c(H+)
����ѧ���á�
����1����0.1 mol��L��1��NH4Cl��Һ
����������_________________________________________��
����С��ϵ______________________________(H2O����)��
�������غ�_________________________________________��
������NH4Cl===NH��Cl��(��ȫ����)
NH��H2O�PNH3��H2O��H��(��)
H2O�PH����OH��(����)
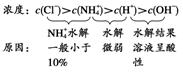
������Cl����NH��H����NH3��H2O��OH����H2O
��c(Cl��)>c(NH)>c(H��)>c(OH��)
��c(Cl��)��c(NH)��c(NH3��H2O)
����2����0.1 mol��L��1��NaHCO3��Һ�и�����Ũ�ȵĹ�ϵ
����С��ϵ________________________________��
�������غ�________________________________��
������غ�________________________________��
�������غ�________________________________��
������NaHCO3===Na����HCO(��ȫ����)
HCO��H2O�PH2CO3��OH��(��Ҫ)
HCO�PH����CO(��Ҫ)
H2O�PH����OH��(����)
������c(Na��)>c(HCO)>c(OH��)>c(H��)>c(CO)
��c(Na��)��c(HCO)��c(CO)��c(H2CO3)
��c(Na��)��c(H��)��c(HCO)��2c(CO)��c(OH��)
��c(OH��)��c(H2CO3)��c(H��)��c(CO)
����3����0.1 mol��L��1��Na2CO3��Һ�и�����Ũ�ȵĹ�ϵ
����С��ϵ_______________________________��
�������غ�_______________________________��
������غ�_______________________________��
�������غ�_______________________________��
������Na2CO3===2Na����CO(��ȫ����)
CO��H2O�PHCO��OH��(��Ҫ)
HCO��H2O�PH2CO3��OH��(��Ҫ)
H2O�PH����OH��(����)
������c(Na��)>c(CO)>c(OH��)>c(HCO)>c(H��)
��c(Na��)��2{c(CO)��c(HCO)��c(H2CO3)}
��c(Na��)��c(H��)��c(HCO)��c(OH��)��2c(CO)
��c(OH��)��c(H��)��2c(H2CO3)��c(HCO)
7���ж��������������ǿ���ķ���
��֪����Һ�������ǿ��(��pH�Ĵ�С)���ж����ɸ�����Ӧ�������ǿ����������ǣ�
ǿ����������Һ�ļ�Խǿ������Ӧ��������Ծ�Խ����ǿ����������Һ������Խǿ������Ӧ����ļ��Ծ�Խ����
8���ж���ʽ����Һ������Եķ���
��ʽ�ε�ˮ��Һ��ʲô���ʣ���Ҫ�����ε�����������ʡ����������������ˮ���ˮ�����أ�����������ʽ������ӣ���ô��ʽ���������ˮ��Һ�мȿ��Ե����ֿ���ˮ�⡣
��ǿ�����ʽ��ֻ���룬��ˮ�⣬һ�������ԡ�
������������ռ���ƣ��������ԣ���NaHSO3��NaH2PO4-�ȣ����ˮ������ռ���ƣ����ԼNaHCO3��NaHS��Na2HPO4�ȡ�
����ѧ������
1����ͬŨ�ȵ�������Һ��pH��С�����˳�����У���NaCl����NaHCO3���� Na2CO3����NaOH����NaHSO4����NH4Cl����H2SO4����Ba(OH)2.
���𰸣���������������������������������
2���Ƚ�������Һ��
����֪ͬŨ�ȵ�NaX��NaY��NaZ��Һ,��������ǿ��������ǿ��˳��Ϊ�������������𰸣�HX>HY>HZ��
����֪AOH��BOH��COH�ļ������μ�������ͬŨ�ȵ�ACl��BCl��CCl��Һ��pH�ɴ�С��˳��Ϊ�� �����𰸣�ACl> BCl>CCl��
��̽���߿���
1��[2012���������ۣ�23(3)]��֤��Na2SO3��Һ�д���SO��H2O���HSO��OH��ˮ��ƽ�����ʵ��____________(�����)��
A�������̪��Һ��죬�ټ���H2SO4��Һ���ɫ��ȥ
B�������̪��Һ��죬�ټ�����ˮ���ɫ��ȥ
C�������̪��Һ��죬�ټ���BaCl2��Һ����������Һ�ɫ��ȥ
����C
������Na2SO3��Һ�����̪��Һ��죬˵��SO������ˮ�ⷴӦ����Һ�Լ��ԡ�����H2SO4��Һ��SO��H������HSO��HSO��H����Ӧ�ų�SO2���壬ͬʱH���к�SOˮ�������OH������ʹ��Һ�в�����ˮ��ƽ�⣬��Һ��ɫҲ����ȥ����A������ˮ�������Ժ�ǿ�����ԣ�������ˮ��Cl2��HClO����SO��HSO����SO��H���к�SOˮ�������OH����HClO����Ư��ָʾ����̪������������SOˮ�ⷴӦ�Ŀ����ԣ���B��������BaCl2��Һ��Ba2����SO�������BaSO3������c(SO)��С����Һ�ĺ�ɫ��ȥ��˵����Һ��c(OH��)��С��ˮ��ƽ�������ƶ���֤������SO��ˮ��ƽ�⣬��C��ȷ��
2��(2012���Ĵ����ۣ�10)�����£�������Һ�е���Ũ�ȹ�ϵ��ȷ���� (����)
A��������ˮ�м������NaOH��c(Na��)��c(Cl��)��c(ClO��)��c(OH��)
B��pH��8.3��NaHCO3��Һ��c(Na��)>c(HCO)>c(CO)>c(H2CO3)
C��pH��11�İ�ˮ��pH��3������������ϣ�c(Cl��)��c(NH)>c(OH��)��c(H��)
D��0.2 mol��L��1 CH3COOH��Һ��0.1 mol��L��1 NaOH��Һ�������ϣ�2c(H��)��2c(OH��)��c(CH3COO��)��c(CH3COOH)
����D
������Ҫ��������Һ�е��غ���⡣���κ���Һ�ж����ڵ���غ㣬ѡ��A����Һ�е���غ�Ϊc(Na��)��c(H��)��c(ClO��)��c(Cl��)��c(OH��)����A����NaHCO3��Һ��pH��8.3��˵����ˮ��̶ȴ��ڵ���̶ȣ���c(H2CO3)>c(CO)����B����pH��11�İ�ˮ��pH��3�������������ʱ����ˮ�ǹ����ģ���Һ�������ԣ���C����Dѡ���е�CH3COOH��NaOH��Ӧ���õ����ǵ�Ũ�ȵ�CH3COOH��CH3COONa�Ļ����Һ���ɵ���غ�ã�c(CH3COO��)��c(OH��)��c(H��)��c(Na��)����Ԫ���غ��2c(Na��)��c(CH3COO��)��c(CH3COOH)��������غ��ϵʽ����2��Ԫ���غ��ϵʽ��ӵã�c(CH3COO��)��2c(OH��)��2c(H��)��c(CH3COOH)������ã�2c(H��)��2c(OH��)��c(CH3COO��)��c(CH3COOH)����D��ȷ��
3��(2012���������ۣ�12)�������һ�����ᣬ��������ʴ��������֪25 ��ʱ��
��HF(aq)��OH��(aq)===F��(aq)��H2O(l) ��H����67.7 kJ��mol��1
��H��(aq)��OH��(aq)===H2O(l) ��H����57.3 kJ��mol��1
��20 mL 0.1 mol��L��1������м���V mL 0.1 mol��L��1 NaOH��Һ�������й�˵����ȷ���� (����)
A�������ĵ��뷽��ʽ����ЧӦ�ɱ�ʾΪHF(aq)�PF��(aq)��H��(aq)����H����10.4 kJ��mol��1
B����V��20ʱ����Һ�У�c(OH��)��c(HF)��c(H��)
C����V��20ʱ����Һ�У�c(F��)<c(Na��)��0.1 mol��L��1
D����V>0ʱ����Һ��һ�����ڣ�c(Na��)>c(F��)>c(OH��)>c(H��)
����B
�����������ʱӦ�ر�ע�⣬HF�����ᣬ����Һ�в�����ȫ���룻��Һ������Ũ�ȴ�С���ж�Ҫ������õ���غ�������غ㡣���ݸ�˹���ɣ�����ʽ��ȥ��ʽ�ɵã�HF(aq)�PH��(aq)��F��(aq)����H����10.4 kJ��mol��1����A�����V��20ʱ������ǡ����ȫ��Ӧ����NaF����Һ�д��������غ��ϵ��c(OH��)��c(HF)��c(H��)����F��ˮ�⣬����Һ�д��ڣ�c(F��)<c(Na��)��0.05 mol��L��1����B����ȷ��C�����D���Һ������Ũ�ȵĴ�Сȡ����V�Ĵ�С����Һ�ȿ��ܳ����ԣ�Ҳ���ܳʼ��ԣ���D�����
4��(2010���㶫���ۣ�12)HAΪ������ǿ�ڴ����һԪ���ᣬ��0.1 mol��L��1 NaA��Һ�У�����Ũ�ȹ�ϵ��ȷ���� (����)
A��c(Na��)>c(A��)>c(H��)>c(OH��) B��c(Na��)>c(OH��)>c(A��)>c(H��)
C��c(Na��)��c(OH��)��c(A��)��c(H��) D��c(Na��)��c(H��)��c(A��)��c(OH��)
�𰸡�D
5��(2010���������ۣ�13)��0.01 mol�������ʷֱ����100 mL ����ˮ�У��ָ������£�������Һ��������Ũ�ȵĴ�С˳����(��Һ����仯���Բ���) (����)
��Na2O2����Na2O����Na2CO3����NaCl
A����>��>��>�� B����>��>��>��
C��������>��>�� D��������>������
����C
6��(2011���������ۣ�13)�����£���1.000 mol��L��1�������20.00 mL 1.000 mol��L��1��ˮ�У���ҺpH���¶��������������仯��������ͼ��ʾ�������й�˵����ȷ����(����)
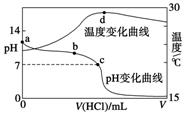
A��a����ˮ�������c(H��)��1.0��10��14 mol��L��1
B��b�㣺c(NH)��c(NH3��H2O)��c(Cl��)
C��c�㣺c(Cl��)��c(NH)
D��d�����Һ�¶����½�����Ҫԭ����NH3��H2O��������
����C
������a��ʱ��ˮ�е�H��ȫ������ˮ�ĵ��룬��ʱpH<14����c(H��)>1.0��10��14 mol��L��1��A����b��ʱ��Һ�Լ��ԣ���ˮ������c(NH)��c(NH3��H2O)>c(Cl��)��B����c��ʱpH��7����c(H��)��c(OH��)�����ݵ���غ㣺c(Cl��)��c(OH��)��c(NH)��c(H��)���Ƴ�c(Cl��)��c(NH)��C��ȷ��d�����Ҫ����NH��ˮ�ⷴӦ���÷�Ӧ���ȣ�D����
7��[2011��ɽ�����ۣ�29(3)]Na2S��Һ������Ũ���ɴ�С��˳��Ϊ________�������Һ�м�����������CuSO4����ҺpH____(������������������������������)��Na2S��Һ���ڷ�������������ԭ��Ϊ________(�����ӷ���ʽ��ʾ)��
����c(Na��)��c(S2��)��c(OH��)��c(HS��)��c(H��)������2S2����O2��2H2O===2S����4OH��
������Na2S��Һ������Ũ�ȵĴ�С�ɸ�������ˮ��ԭ����������Na2S��CuSO4��Һ��Ӧ��Na2S��CuSO4===CuS����Na2SO4����Һ��pH��С��Na2S��Һ���ڷ��ûᱻ�����е���������Ϊ��2S2����O2��2H2O===2S����4OH����
8��[2011���������ۣ�23��(5)]ϡ��Ԫ���DZ����ս����Դ���ҹ����̲�����������λ����(Ce)�ǵؿ��к�����ߵ�ϡ��Ԫ�ء��ڼ���������CeCl3����ˮ�⣬��ˮCeCl3���ü���CeCl3��6H2O��NH4Cl��������ķ������Ʊ������У�NH4Cl��������________��
�����ֽ���Ȼ������壬����CeCl3ˮ��(������������)
���������ڼ���ʱ�Ȼ�立ֽ���Ȼ������壬��������CeCl3��ˮ�⡣
9��[2012��ɽ�����ۣ�29(4)]NO2���ð�ˮ��������NH4NO3,25 ��ʱ����a mol NH4NO3����ˮ����Һ�����ԣ�ԭ����__________________(�����ӷ���ʽ��ʾ)�������Һ�μ�b L��ˮ����Һ�����ԣ���μӰ�ˮ�Ĺ�����ˮ�ĵ���ƽ�⽫________(����������������������������)�ƶ������μӰ�ˮ��Ũ��Ϊ________mol��L��1��(NH3��H2O�ĵ���ƽ�ⳣ��ȡKb��2��10��5 mol��L��1
����NH��H2O�PNH3��H2O��H��������
������NHˮ��ʹNH4NO3��Һ�����ԣ�NH��H2O�PNH3��H2O��H�����μӰ�ˮʱˮ�ĵ���ƽ�⽫�����ƶ�����Һ�����ԣ��ɵ���غ��֪c(NH)��c(H��)��c(NO)��c(OH��)����n(NH)��n(H��)��n(NO)��n(OH��)����Ϊƽ�����Һ�����ԣ�n(H��)��n(OH��)����n(NH)��n(NO)��a mol�������İ�ˮ��Ũ��Ϊc mol��L��1����Ӧ����Һ���ΪV L��
��Kb������2��10��5 mol��L��1����c����
���̺�ǡ�
������ѵ����
����һ��������ˮ��ʵ�ʼ����ɵĿ���
1��NH4Cl��Һ��________�������ӷ���ʽ��ʾԭ��____________________________��
�����£�pH��11��CH3COONa��Һ�У�ˮ���������c(OH��)��__________����pH��3��CH3COOH��Һ�У�ˮ���������c(H��)��____________��
�������ԡ�NH��H2O���NH3��H2O��H��
10��3 mol��L��1��10��11 mol��L��1
������NH4ClΪǿ�������Σ�����NHˮ������ԣ�CH3COONa��Һ������
CH3COO��ˮ��ٽ�ˮ�ĵ��룬��pH��11��CH3COONa��Һ�У�c(OH��)ˮ��10��3 mol��L��1����pH��11��CH3COOH��Һ��ˮ�ĵ����ܵ����ƣ���c(H��)ˮ��10��11
mol��L��1��
2�����������ʵ���Ũ������Ҷ���һ��������A����B����һ��������X����Y����ɵ�����Һ���ݲⶨ������AX��BY��Һ��pH��7��AY��Һ��pH>7��BX��Һ��pH<7���ɴ��жϲ�ˮ������� (����)
A��BX B��AX C��AY D��BY
�𰸡�B
������AY��Һ��pH>7��˵��AYΪǿ�������Σ�BX��Һ��pH<7��˵��BXΪǿ�������Σ���AXΪǿ��ǿ���Σ����ܷ���ˮ�⣬B�ԡ�
3������Na2CO3��Һ����CH3COONa��Һ����NaOH��Һ��25 mL�����ʵ���Ũ�Ⱦ�Ϊ0.1 mol��L��1������˵����ȷ���� (����)
A��������ҺpH�Ĵ�С˳������>��>��
B������������Һϡ����ͬ������pH�仯��������
C�����ֱ����25 mL 0.1 mol��L��1�����pH��������
D����������Һ��pH��Ϊ9�������ʵ���Ũ�ȵĴ�С˳����>��>��
����C
�������������Խ��Խ��ˮ�⣬���������ҺpH�Ĵ�С˳��Ӧ����>��>��������������Һϡ����ͬ����������Na2CO3��Һ��CH3COONa��Һ�д���ˮ��ƽ�⣬����ˮ�ļ�����������ӻ�ˮ�����������OH�������pH�仯����Ӧ������ѡ��D��ȷ��˳��ӦΪ��>��>����
���������ˮ�����ӷ���ʽ�Ŀ���
4�����з�Ӧ������ˮ�ⷴӦ��ˮ�ⷽ��ʽ����ȷ���� (����)
��HCl��H2O���H3O����Cl��
��AlCl3��3H2O===Al(OH)3��3HCl
��Na2CO3��2H2O���H2CO3��2NaOH
��̼��������Һ��HCO��H2O���CO��H3O��
��NH4Cl����D2O��NH��D2O���NH3��D2O��H��
A���٢ڢۢ� B���٢ڢ�
C���ڢۢ� D��ȫ��
����D
�������٢��ǵ��뷽��ʽ����Ӧ����===��������ˮ�ⷴӦ����ʽ����Ӧ���������������ˮ�ⷽ��ʽ����Ӧ�ֲ����У���ӦΪNH��D2O���NH3��HDO��D����
5������������ˮ������MnRm��Һ����pH>7����ԭ����_______________________��
��pH<7����ԭ����___________________________________________________��
(ע���������������ӷ���ʽ˵��)
����Rn����H2O���HR(n��1)����OH��
Mm����mH2O���M(OH)m��mH��
������pH����7�������������ˮ��ʼ��ԣ�pHС��7����������������ˮ������ԡ�
����һ�������ı�ʱˮ��ƽ���ƶ�������ж�
1����CH3COONaϡ��Һ�м���(��ͨ��)����X���ʣ�����Һ�в�������Ũ�ȱ仯�����ʾ(��Һ�¶Ȳ���)��X���������������е� (����)
|
�� |
H�� |
OH�� |
CH3COO�� |
CH3COOH |
|
���ʵ� ��Ũ�� |
���� |
��С |
��С |
���� |
A���������� B���Ȼ���
C������ˮ D��������
����B
��������CH3COONaϡ��Һ�м����������ƣ�c(OH��)����������ˮ��c(CH3COOH)��С�����������ƣ�����CH3COO��ˮ�⣬c(CH3COO��)����
2����һ�������£�Na2CO3��Һ����ˮ��ƽ�⣺CO��H2O���HCO��OH��������˵����ȷ���� (����)
A��ϡ����Һ��ˮ��ƽ�ⳣ������
B����������NH4Cl���壬ƽ�⳯����Ӧ�����ƶ�
C�������¶ȣ���С
D������NaOH���壬��ҺpH��С
����B
��������ѧƽ�ⳣ��ֻ���¶ȵ�Ӱ�죬A�������NH4Cl����������NH��OH����Ӧ��ʹƽ��������Ӧ�����ƶ���B��ȷ���¶����ߣ�CO��ˮ��̶�����c(HCO)����c(CO)��С��C������NaOH���壬��Һ��pH����D����
�������ѡȡ��ʩʹˮ��ƽ�ⶨ���ƶ�
3����ͼ��ʾ������ƿ�зֱ�װ�뺬��̪��0.01 mol��L��1 CH3COONa��Һ�����ֱ������ʢ��ˮ���ձ��У�Ȼ�����ձ����м�����ʯ�ң����ձ����м���NH4NO3���壬�ձ����в����κ����ʡ�

(1)����̪��0.01 mol��L��1 CH3COONa��Һ��dz��ɫ��ԭ��Ϊ__________________��
(2)ʵ������з�����ƿ������Һ��ɫ�����ƿ������Һ��ɫ��dz��������������ȷ����________��
A��ˮ�ⷴӦΪ���ȷ�Ӧ
B��ˮ�ⷴӦΪ���ȷ�Ӧ
C��NH4NO3����ˮʱ�ų�����
D��NH4NO3����ˮʱ��������
(3)��0.01 mol��L��1 CH3COONa��Һ�зֱ����NaOH���塢Na2CO3���塢FeSO4���壬ʹCH3COO��ˮ��ƽ���ƶ��ķ���ֱ�Ϊ____________��____________��____________��(�����������������������ƶ���)
�𰸡�(1)CH3COO����H2O���CH3COOH��OH����ʹ��Һ�Լ��ԡ�(2)BD��(3)������
������(1)CH3COONa��CH3COO��ˮ��ʹ��Һ�Լ��ԣ���̪��Һ�����Ժ�ɫ��
(2)��ʯ����ˮ���ҷ�Ӧ�ų������ȣ�������ƿ������Һ��ɫ����ж�ˮ��ƽ�������ƶ���˵��ˮ�ⷴӦ�����ȷ�Ӧ��ͬʱ��ƿ������Һ��ɫ��dz����NH4NO3����ˮʱ����������
(3)������CH3COO����ˮ�⣻COˮ���Լ��ԣ���CH3COO����ˮ������ƣ�
Fe2��ˮ�������ԣ���CH3COO����ˮ����ٽ���
����һ������Һ�������ò�����ж�
1��(1)̼��ص�ˮ��Һ���ɵõ��Ĺ���������__________________��ԭ����__________��
(2)KAl(SO4)2��Һ���ɵõ��Ĺ���������________��ԭ����___________________��
(3)̼��������Һ���ɵõ��Ĺ���������________��ԭ����_________________��
(4)����������Һ���ɵõ��Ĺ���������________��ԭ����____________________��
(5)�����������1 mol��L��1�Ļ����10 mL������Ũ����1 mL��������ҺΪ______��ԭ����_______________________________��
����(1)K2CO3�����ܼ��ȹ��̴ٽ�ˮ�⣬�����ɵ�KHCO3��KOH��Ӧ��������K2CO3
(2)KAl(SO4)2��12H2O������Al3��ˮ�⣬������H2SO4Ϊ�ѻӷ����ᣬ�����ȻΪ�ᾧˮ���ע���¶ȹ��ߣ�����ȥ�ᾧˮ
(3)Na2CO3��2NaHCO3Na2CO3��CO2����H2O
(4)Na2SO4��2Na2SO3��O2===2Na2SO4
(5)H2SO4��Һ��HCl�ӷ�
�����������漰��֪ʶ��Χ�Ϲ��������ε�ˮ��������Ӧ���ǵ��ε����ȶ�������ԭ�Եȡ�
�����������ˮ��ƽ���ƶ�����ʵ������
2����ͨ��ĭ������ĸ���������װ��һֻС����Ͳ������Ͳ��ʢװ��������Һ������������ʢװ̼�����Ʊ�����Һ��ʹ��ʱ�����������������ҩҺ���Ͼͻ������������̼�İ�ɫ��ĭ��
(1)��������������ӷ���ʽ��______________________________________��
(2)���ܰ���������Һװ����Ͳ�����Ҫԭ����_______________________��
(3)һ�㲻��̼���ƴ���̼�����ƣ�����Ϊ___________________________��
����(1)Al3����3HCO===Al(OH)3����3CO2��
(2)Al2(SO4)3��Һ��ˮ������ԣ��ḯʴ����
(3)���ᷴӦ����NaHCO3>Na2CO3����������CO2ʱ��Na2CO3����Al3������
������(1)Al3����HCO����˫ˮ�ⷴӦAl3����3HCO===Al(OH)3����3CO2����
(2)Al2(SO4)3��Һ��ˮ�����������ʴ������Al3����3H2O���Al(OH)3��3H����Fe��2H��===Fe2����H2����
(3)���ᷴӦ����NaHCO3>Na2CO3����������CO2ʱ������Al3������Na2CO3>NaHCO3����������Na2CO3��NaHCO3�ֱ�������Al3����Ӧ������CO2��NaHCO3>Na2CO3��
3����֪H2O2��KMnO4��NaClO��K2Cr2O7������ǿ�����ԡ�
����Һ�е�Cu2����Fe2����Fe3������Ϊ�����������Һ��pH�ֱ�Ϊ6.4��9.6��3.7�����к�FeCl2���ʵ��Ȼ�ͭ����(CuCl2��2H2O)��Ϊ��ȡ������CuCl2��2H2O�����Ƚ����Ƴ�ˮ��Һ��Ȼ��ͼʾ��������ᴿ��
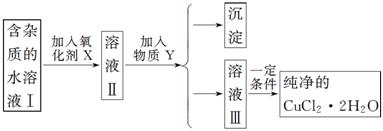
��ش��������⣺
(1)��ʵ�����ʺϵ�������X��________(�����)��
A��K2Cr2O7 B��NaClO
C��H2O2 D��KMnO4
(2)����Y��________��
(3)��ʵ���üӼ�������ܲ��ܴﵽĿ�ģ�______��ԭ����
____________________________________________________________________��
(4)��ȥFe3�����й����ӷ���ʽ��______________________________________��
(5)����������Ŀ����_________________________________________________��
(6)����ܲ���ֱ�������ᾧ�õ�CuCl2��2H2O���壿________��Ӧ��β�����_____________________________________________________________________��
����(1)C
(2)CuO[��Cu(OH)2��CuCO3��Cu2(OH)2CO3]
(3)���ܡ���Ӽ��ͬʱҲ��ʹCu2������Cu(OH)2����
(4)Fe3����3H2O���Fe(OH)3��3H����CuO��2H��===Cu2����H2O[��Cu(OH)2��2H��
===Cu2����2H2O��]
(5)��Fe2������ΪFe3�����������ɳ�������Cu2������
(6)���ܡ�Ӧ��HCl�����м�������
������(1)�ܰ�Fe2������ΪFe3����ͬʱ�ֲ��������µ����ʣ�����Ҫ���ֻ��H2O2��(2)��CuCl2��Һ�л���Fe3��ʱ����������Fe3����ˮ�⣺Fe3����3H2O���Fe(OH)3��
3H��������CuO��Cu(OH)2��CuCO3��Cu2(OH)2CO3����Һ�е�H�����ã��Ӷ�ʹˮ��ƽ�����ƣ�ʹFe3��ת��ΪFe(OH)3��������ȥ��(3)���üӼʹFe3��������ͬʱҲ�ؽ�ʹCu2��������(6)Ϊ������CuCl2ˮ�⣬Ӧ��HCl�����м���������
���������й�����Һ�����Ƽ�����Ŀ���
4������������Һʱ����������������ڵ����ʣ����в���Ϊ����������ˮ�����(����)
A��FeSO4(Fe) B��SnCl2(HCl)
C��FeCl3(HCl) D��NaAlO2(NaOH)
����A
������A���м�����м�Ƿ�ֹFe2����������
5������BiCl3��Һʱ��ˮ�����BiOCl���ɶ�ʹ��Һ�ʻ�������
(1)д������������ķ�Ӧ����ʽ��____________________________________��
(2)ҽҩ�ϳ���BiOCl��Ϊ�������飬������________(������ȷ����������ȷ��)��
(3)�������BiCl3��Һ��______________________________________________��
����(1)BiCl3��H2O===BiOCl����2HCl
(2)����ȷ��(3)������BiCl3�����ܽ�������Ũ�����У�Ȼ���ˮϡ��
�����ġ���ˮ���йص����ӹ�������
6����ɫ����Һ���ܴ���������������� (����)
A��Na����Al3����HCO��NO
B��AlO��Cl����Mg2����K��
C��NH��Na����CH3COO����NO
D��Na����NO��ClO����I��
����C
������A�Al3������HCO����˫ˮ�ⷴӦ���ܴ������棻B�AlO��Mg2����Ӧ����Mg(OH)2��Al(OH)3�������ܴ������棻C�NH��CH3COO�����ܷ���˫ˮ�ⷴӦ�����ܴ������棻D�ClO����I���ܷ���������ԭ��Ӧ���ܴ������档
7������ָ����Һ��һ���ܴ���������������� (����)
A��pH��1����Һ�У�NH��Na����Fe3����SO
B�����д���AlO����Һ�У�Na����K����HCO��NO
C��������Һ�У�K����Al3����Cl����SO
D��Na2S��Һ�У�SO��K����Cu2����Cl��
����A
������A����������£�H������NH��Fe3����ˮ�⣬�ܴ������棻B�AlO��HCO��H2O===Al(OH)3����CO�����ܴ������棻C�Al3��ˮ������ԣ������������Һ�в����ڣ�D�Cu2����S2��===CuS�������ܴ������档
����ȴ�������
��һƪ����ʮһ��Ԫ ˮ��Һ�е�����ƽ�⣨3��
��һƪ����ʮһ��Ԫ ˮ��Һ�е�����ƽ�⣨5��
