��ʮһ��Ԫ ˮ��Һ�е�����ƽ�⣨3��
2015-11-25 09:49:37 ��Դ�� �壺��Х ��Ӱ���� ; ���ۣ�0 �����
��ʮһ��Ԫ ˮ��Һ�е�����ƽ�⣨3��
|
|
|
�ڿ��ˣ��� Х |
|
|
������ԭ����ƽ��ԭ��������ˮ���ԭ���� |
|
|
��ѧĿ�꣺ |
��������ҺpH��������Ũ�ȡ�����������Ũ�ȵļ��㣻 |
|
|
|
������ƽ���ƶ�ԭ������ijЩ���⡣
|
|
|
��ѧ�ص㣺 |
ҺpH��������Ũ�ȡ�����������Ũ�ȵļ��� |
|
|
��ѧ�ѵ㣺 |
����ƽ���ƶ�ԭ������ijЩ���� |
|
|
��ѧ������ |
���������������Ƚϣ����ֹ��� |
|
|
��ѧ���̣� |
������ʱ |
|
����֪ʶ����
��������к͵ζ�
1�����壺��������кͷ�Ӧ������֪Ũ�ȵ���(���)���ⶨδ֪Ũ�ȵļ�(����)��ʵ�鷽����������к͵ζ���
2��ԭ�������ǡ����ȫ��Ӧ����ͼ����������ݻ�ѧ����ʽ�е���ͼ�����ʵ���֮�ȣ�ͨ������ó�δ֪��Һ��Ũ�ȡ�
C(��)��V(��)=c(��)��V(��) (һԪ���)
3���ɹ��Ĺؼ���
��ȷ�ⶨ������Һ���������ȷ�жϵζ��յ㡣
4����������:
����������ʽ�ζ��ܡ���ʽ�ζ��ܡ���ƿ������̨���ζ��ܼС��ձ��ȡ�
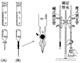
��ʽ�ζ��ܣ�����ʢ�ż�Һ��ˮ������Ե�����Һ���������
��ʽ�ζ��ܣ�����ʢ��������Һ��ǿ��������Һ��
���Լ�������Һ��������Һ������ˮ��ָʾ��
����չ֪ʶ��
ָʾ����ѡ��ѡ��ָʾ��ʱ���ζ��յ�ǰ����Һ����ɫ�ı䣬��ɫ�仯�Ա����ԣ���ɫ��Χ������ζ��յ���Һ�������һ�¡�
�������ָʾ������ɫ��Χ
|
ָʾ�� |
��ɫ��Χ��pH |
|
|
|
ʯ�� |
<5.0��ɫ |
5.0��8.0��ɫ |
>8.0��ɫ |
|
���� |
<3.1��ɫ |
3.1��4.4��ɫ |
>4.4��ɫ |
|
��̪ |
<8.2��ɫ |
8.2��10.0dz��ɫ |
>10.0��ɫ |
(1)ǿ����ǿ����к͵ζ��������յ�ʱ��pH�仯��Χ�ܴ�һ���÷�̪��Ҳ���ü��ȡ�
(2)ǿ��ζ�����ǡ����ȫ��Ӧʱ�����ɵ���ˮ��ʹ��Һ�����ԣ���ѡ�������Է�Χ�ڱ�ɫ��ָʾ���������ȡ�
(3)ǿ��ζ����ᣮǡ����ȫ��Ӧʱ�����ɵ���ˮ��ʹ��Һ�ʼ��ԣ���ѡ���ڼ��Է�Χ�ڱ�ɫ��ָʾ��������̪��
ע�⣺һ�㲻��ʯ����Һ��ԭ��������Һ��ɫ�仯�ԱȲ����ԣ��ұ�ɫ��Χ�ϴ�
���������̣�
a.�����ζ��ܣ���©����ϴ��װҺ�����㣩����ƿ��ϴ�ӡ�ȡҺ����������ָʾ������
b.�ζ������ζ����е�Һ��������ƿ�У��ȿ��������ֱ��ָʾ������ɫǡ�÷����仯�Ұ���Ӳ��仯Ϊֹ����¼�������ݣ����ظ���2��3�Σ�
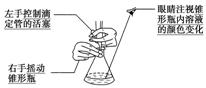
c.���������������ݴ��빫ʽ���м��㡣
��ע�⡿
a.һ�����Һװ����ƿ�У���Һװ�ڵζ����У�
b.��ƿ������ϴ��
c.�ζ��������������ջ�����ת���أ����ֲ�����ת����ƿ���۾�ע����ƿ����ɫ�仯��
d.�ζ��������ʱӦȡƽ��ֵ��
5��������:
���������ݣ�![]() (a��ʾ����Ӧ�Ļ�ѧ��������)
(a��ʾ����Ӧ�Ļ�ѧ��������)
�������������Դ���Һ������ƿΪ����
ʵ�ʲ����п��ܻ�����c����V����V���ı仯�����ڼ���ʱ��c����V�����ǹ̶�ֵ��������������Ϊ��֪�����㣬ֻ�еζ����������ĵı�Һ�����V���治ͬ�������仯����V����һ��������
����ʱֻҪ��������V����Ӱ����Σ��������ʹV������������Ĵ���Һ��Ũ��ƫ��֮��ƫС��
�����ķ��ࣺ
A.ƫ��
a���ζ���δ��ϴ��ֱ��װ��Һ��
b����ƿˮϴ���ô���Һ��ϴ��
c���ζ�ǰ�ζ����������ݣ��ζ���ζ�����������ʧ��
d���ζ�ʱ��Һ������ƿ�⣻
e���ζ��յ�ʱ���Ӷ�����
f���ζ��յ�ʱ����Һ������
g���ζ���ʼʱ���Ӷ������ζ��յ�ʱ���Ӷ�����
B.ƫ��
a��ȡ����Һ�ĵζ��ܻ���Һ��ˮϴ��δ��ϴ��
b��ȡ����Һʱ����ʧ��
c���ζ��յ�ʱ���Ӷ�����
d���ζ���ʼʱ���Ӷ������ζ��յ�ʱ���Ӷ�����
e����Һ��ɫ�ոճ��ֱ仯��ֹͣ�ζ���
C. ��Ӱ��
a����ƿˮϴ��δ����Ҳδ�ô���Һ��ϴ��
b���ζ��ܵ���ʱ��Һ�������̶ȣ�������ȷ�ģ���
c���ζ�ǰ����ƿ�м�������ˮ��
����ѧ���á��Ա�����Һ�ζ�δ֪Ũ�ȵļ�(��̪��ָʾ��)Ϊ�������������������ȷ�����������У�
|
���� |
���� |
V(��) |
c(����) |
|
ϴ�� |
��ʽ�ζ���δ�ñ���Һ��ϴ |
��� |
ƫ�� |
|
��ʽ�ζ���δ�ô�����Һ��ϴ |
��С |
ƫ�� |
|
|
��ƿ�ô�����Һ��ϴ |
��� |
ƫ�� |
|
|
��ƿϴ������������ˮ |
���� |
��Ӱ�� |
|
|
ȡҺ |
�ų���Һ�ĵζ��ܿ�ʼ�����ݣ��ų�Һ���������ʧ |
��С |
ƫ�� |
|
�ζ� |
��ʽ�ζ��ܵζ�ǰ�����ݣ��ζ��յ�ʱ������ʧ |
��� |
ƫ�� |
|
����ƿʱ����Һ�彦�� |
��С |
ƫ�� |
|
|
������Һ�γ���ƿ�� |
��� |
ƫ�� |
|
|
��Һ��ɫ��dzʱ������Һ���죬ֹͣ�ζ���һ��NaOH��Һ�ޱ仯 |
��� |
ƫ�� |
|
|
���� |
��ʽ�ζ��ܵζ�ǰ������ȷ���ζ����Ӷ���(��ǰ����) |
��С |
ƫ�� |
|
��ʽ�ζ��ܵζ�ǰ������ȷ���ζ������Ӷ���(��ǰ������) |
��� |
ƫ�� |
6�����ⷽ��
�ٵζ��յ���жϴ���ģ�壺���������һ������������������Һ����Һ���������������ɫ���Ұ�����ڲ��ָ�ԭ������ɫ��
��ͼ�������Ķ�������

ƽ�Ӷ�������ͼ1ʵ����������Ͳ����Һ�ܻ�ζ�����ȡһ�������Һ�壻��ȡҺ�����ʱ������Ӧ�밼Һ����͵㱣��ˮƽ��������̶ȵĽ��㼴Ϊ����(����Һ�涨���ߣ����߶�����)��
���Ӷ�����������ͼ2������Ͳ����Һ������ʱ�����ڸ�������������б��Ѱ���е��λ���ڰ�Һ����ϲ࣬����������ȷ�Ŀ̶���λ�ã�������ƫ��
���Ӷ�������ͼ3����ʱ����������������б��Ѱ���е��λ����Һ����²࣬��ζ��̶ܿȱ귨����Ͳ��ͬ���������Ӷ���ƫ��
���Ӻ����ӵ�����Ҫ��Ͼ����������з�������Ϊ��Ͳ�̶ȴ��µ����������ζ��̶ܿȴ��µ�����С�����ҵζ�����Һ�������������������֮��ڷ���ʱ��Ҫ���ζ�ǰ�����Ƿ���ȷ��Ȼ������ж�ʵ����ȡ��Һ�������ƫ����ƫС��
�����˼����
1����ʽ�ζ���������©��
��������ϴ���ĵζ�����װ��һ�������ˮ�������ڵζ��ܼ���ֱ�����������ӣ��۲�����ˮ��©�¡�Ȼ������ת180�����پ��������ӣ��۲�����ˮ��©�£������©ˮ���ζ��ܼ���ʹ�á�
2������Ϊ25 mL�ĵζ��ܣ��ζ���������ȥ10.00 mL��Һ�壬��ʱ�ζ�����ʣ��Һ������Ϊ15 mL��
�𰸡����ڵζ��ܵ���0���̶��ڵζ��ܵ��Ϸ����ζ����¶���û�п̶ȵģ���ʣ��Һ���������15 mL��
3��(1)�ζ���ΪʲôҪ��ϴ����ƿ��Ҫ��ϴ��(2)����ʱΪʲôҪƽ�Ӱ�Һ�棿(3)�ζ����ſ�����Ŀ����ʲô��
����(1)�ζ��ܲ���ϴ�൱�ڶ���ʢװ��Һ��ϡ�ͣ���ƿ������ϴ����ϴ���൱����ʢװ��Һ�����ʵ�������(2)���Ӷ���ƫ���Ӷ���ƫС��(3)�粻�ſ�����ȡҺʱ�����С���ζ�ʱ������
4��KMnO4(H��)��Һ����ˮ��Na2CO3��Һ��ϡ����Ӧ�ֱ�ʢ�������ֵζ����У�
�𰸣�ǿ��������Һ��������ҺӦʢ������ʽ�ζ����У�������ҺӦʢ���ڼ�ʽ�ζ����С�������KMnO4��Һ��ϡ���ᡢ��ˮӦʢ������ʽ�ζ����У�Na2CO3��ҺӦʢ���ڼ�ʽ�ζ����С�
5���ζ���ʢ����Һʱ����Һ��һ��Ҫ��0�̶���
������һ����ֻҪ��0�̶Ȼ�0�̶�����ij�̶ȼ��ɣ���һ��Ҫ��¼�µζ���ʼǰҺ��Ķ�����
6��(1)�к͵ζ��Ĺؼ���ʲô��(2)�ζ��յ�������ǡ���к͵ĵ���
�𰸡�(1)�к͵ζ��Ĺؼ�����ȷ�ⶨ���ַ�Ӧ����Һ���������ȷ����ҺŨ�ȵ�ȷ�����ζ��յ��ȷ�ж�(����ָʾ���ĺ���ѡ��)��
(2)�ζ��յ���ָʾ����ɫ����ͻ��ĵ㣬��һ�������ǡ���к͵ĵ㡣
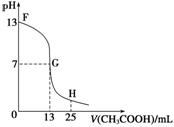 7����ͼΪ����ʱ��25 mLijŨ�ȵ�NaOH��Һ����εμ�0.2 mol��L��1��CH3COOH��Һ�Ĺ�����pH�ı仯���ߡ�
7����ͼΪ����ʱ��25 mLijŨ�ȵ�NaOH��Һ����εμ�0.2 mol��L��1��CH3COOH��Һ�Ĺ�����pH�ı仯���ߡ�
(1)ͼ��NaOH�����ʵ���Ũ��Ϊ_________mol��L��1��
(2)G����Һ�����ԣ������ǡ����ȫ��Ӧ�ĵ�����FG���仹��GH���䣿________���䡣
����(1)0.1��(2)FG
��������NaOH��Һ�еμӴ��ᣬ���pH��13��NaOH��Ũ��Ϊ0.1 mol��L��1������ǡ����ȫ��Ӧʱ������CH3COONa����ʱ��Һ�ʼ��ԣ�Ӧ����FG֮�䡣
��֪ʶ��չ���к͵ζ�����չӦ��
1.�������
(1)���
�����ζ��������ó�����Ӧ���еζ������������ķ��������磬����Ag����±�����ӵķ�Ӧ���ⶨCl����Br����I��Ũ�ȡ�
(2)ԭ����
���ó�����Ӧ���ⶨǡ�÷�Ӧʱ���������ʵ������ͨ������ó�ij�����ʵĺ�����
�ۼ��㣺���ó�����Ӧ����������֮��Ķ�����ϵ��ͨ������ȷ��λ�����ʵĺ�����
��ָʾ���������ζ����õ�ָʾ����������һ�ֳ��������ζ����뱻�ζ��ﷴӦ����������ܽ��Ҫ�ȵζ�����ָʾ����Ӧ����������ܽ��С��������������ָʾ��������AgNO3��Һ�ζ���Һ�е�Cl���ĺ���ʱ����CrOΪָʾ����������ΪAgCl��Ag2CrO4�����ܵ�Ե�ʡ�
2��������ԭ�ζ�
�ٶ��壺��������ԭ��ӦΪ�����IJⶨ������
��ԭ��������������ԭ��Ӧ���ⶨǡ�÷�Ӧʱ���������ʵ������ͨ������ó�ij�����ʵĺ�����
�ۼ��㣺����������ԭ��Ӧ����������֮��Ķ�����ϵ��ͨ������ȷ��λ�����ʵĺ�����
��ָʾ��������������ԭ��Ϊ�ζ�����ֱ�ӵζ�һЩ���л�ԭ�Ի������Ե����ʣ�����ӵζ�һЩ������û�������Ի�ԭ�ԣ�������ijЩ��������ԭ����Ӧ�����ʡ������ζ����и��������Һ���ظ������Һ����ˮ��Һ�ȣ���ԭ�ζ�������������Һ������Ѫ��ˮ��Һ(��ά����C)�ȡ�
˵�������������еĵζ�����ʹ��ָʾ�������ñ���Na2SO3�ζ�KMnO4��Һʱ��KMnO4��ɫ��ȥʱ��Ϊ�ζ��յ㡣
��̽���߿���
1���ж�������ȷ�Ļ����̡�������Ļ�������
(1)25 ����60 ��ʱ��ˮ��pH��� (��)(2012���������ۣ�10B)
������ˮ�ĵ��������ȷ�Ӧ�����£��ٽ�ˮ�ĵ��룬c(H��)����
(2)�к͵�����������ʵ���Ũ�ȵ�����ʹ��������ĵ�n(NaOH)��� (��)
(2012���������ۣ�10C)
(3)���к͵ζ���ʵ���У�����ƿ����ƿ������ˮϴ����ʹ�ã��ζ��ܺ���Һ��������ˮϴ�����뾭�������ϴ��ʹ�� (��)(2011���㽭���ۣ�8C)
����������ƿ����ƿ������ϴ�����ζ��ܻ���Һ������ϴ������ʹ�á�
(4)��0.200 0 mol��L��1 NaOH����Һ�ζ�HCl��CH3COOH�Ļ��Һ(���Һ���������Ũ�Ⱦ�ԼΪ0.1 mol��L��1)��������ʱ����Һ�е���δ����ȫ�к�(��)(2012���㽭���ۣ�12C)
������ǿ����ǿ����Һ������ȫ�к�ʱ��������ҺpH��7����ǿ��������������ȫ�к�ʱ����Һ��pH>7����������Һ��pH��7�����㡣
(5)��֪һ���¶��£�������Һ�����ʵ���Ũ��Ϊc�������Ϊ����Ka��������������CH3COONa���壬�����ƽ��CH3COOH���CH3COO����H�������ƶ�������С��Ka��С (��)(2011���㽭���ۣ�12B)
������������Һ�м�������CH3COONa���壬��Һ��c(CH3COO��)����ƽ�����ƣ�����С�������¶Ȳ��䣬Ka���䡣
(6)�����£���pH��3�Ĵ�����Һϡ�͵�ԭ�����10������Һ��pH��4 (��)
(2012���㽭���ۣ�12A)
������ϡ��10����3<pH<4��
(7)25 ��ʱNH4Cl��Һ��Kw����100 ��ʱNaCl��Һ��Kw (��)(2011��������ۣ�5A)
�������¶�Խ�ߣ�KwԽ��
(8)100 ��ʱ����pH��2��������pH��12��NaOH��Һ�������ϣ���Һ������(��)
(2011��������ۣ�5D)
����������100 ��ʱ��Kw>10��14������pH��12��NaOH�������ʼ��ԡ�
(9)�к͵ζ�ʵ��ʱ���ô���Һ��ϴ��ƿ (��)(2012��ɽ�����ۣ�11A)
��������ƿ������ϴ��
2��(2012���Ϻ���7)ˮ�м���������Һ��ˮ�ĵ���ƽ�ⲻ����Ӱ����� (����)
A��NaHSO4��Һ B��KF��Һ C��KAl(SO4)2 ��Һ D��NaI��Һ
����D
������NaHSO4�������ɵ�H��������ˮ�ĵ��룬ѡ��A����KF�������ɵ�F����ˮ�������������HF���Ӷ��ٽ�ˮ�ĵ��룬ѡ��B����KAl(SO4)2�������Al3����ˮ������Al(OH)3���Ӷ��ٽ�ˮ�ĵ��룬ѡ��C����NaI��ǿ��ǿ���Σ���ˮ�⣬�ҵ������Na����I����ˮ�ĵ���ƽ��û��Ӱ�죬ѡ��D��ȷ��
3��(2011���Ĵ����ۣ�9)25 ��ʱ���ڵ��������pH��0��H2SO4��Һ����0.05 mol��L��1��Ba(OH)2��Һ����pH��10��Na2S��Һ����pH��5��NH4NO3��Һ�У����������ˮ�����ʵ���֮���� (����)
A��1��10��1010��109 B��1��5��5��109��5��108
C��1��20��1010��109 D��1��10��104��109
�𰸡�A
������25 ��ʱ��pH��0��H2SO4��Һ����ˮ�������c(H��)��10��14mol��L��1��0.05 mol��L��1��Ba(OH)2��Һ��c(OH��)��0.05 mol��L��1��2��0.1 mol��L��1������Kw��c(H��)��c(OH��)��1.0��10��14������ˮ�������c(H��)��10��13 mol��L��1��pH��10��Na2S��Һ����ˮ�������c(H��)��10��4 mol��L��1��pH��5��NH4NO3��Һ����ˮ�������c(H��)��10��5mol��L��1���ʵ����������Һ�з��������ˮ�����ʵ���֮��Ϊ10��14��10��13��10��4��10��5��1��10��1010��109����ѡ��A��ȷ��
4��(2012���¿α�ȫ������11)��֪�¶�Tʱˮ�����ӻ�����ΪKw�����¶��£���Ũ��Ϊa mol��L��1��һԪ��HA��b mol��L��1��һԪ��BOH�������ϣ����ж�����Һ�����Ե������� (����)
A��a��b B�������Һ��pH��7 C�������Һ�У�c(H��)�� mol��L��1
D�������Һ�У�c(H��)��c(B��)��c(OH��)��c(A��)
����C
�������ж���Һ�����Ե�������c(H��)��c(OH��)��A���У�a��b�����ǡ����ȫ��Ӧ�������κ�ˮ���������ǿ��δ֪������ȷ����Һ������ԣ�B����δ˵���¶�Ϊ25 �����ʻ����Һ��pH��7ʱ��һ�������ԣ�C������Һ�У�c(H��)��c(OH��)��Kw����Ϊc(H��)�� mol��L��1����c(OH��)�� mol��L��1��c(H��)��c(OH��)������Һ�����ԣ�D����c(H��)��c(B��)��c(OH��)��c(A��)��ֻ��˵����Һ�е���غ㣬���ж���Һ������ԡ�
5��(2011���Ϻ���19�ı�)��������pHΪ3��ij����Һ�ֱ���pH��Ϊ11�İ�ˮ������������Һ�������ϵõ�a��b������Һ��������������Һ����Ե�������ȷ����(����)
A��b�����Լ��� B��a���������Ի����
C��a������������ D��b�����Լ��Ի�����
�𰸡�B
������������pHΪ3��ij����Һ������ǿ����ҺҲ������������Һ������ǿ����Һ����pHΪ11�İ�ˮ�������ϣ��õ���a��Һ�Լ��ԣ�����������Һ����pHΪ11�İ�ˮ�������ϣ��õ���a��Һ�������������Ͱ�ˮ�ĵ���̶ȵ���Դ�С��������˿��������ԣ�Ҳ�����Լ��ԡ���֮��a��Һ���������ԣ�Ҳ�����Լ��ԣ���B����ȷ��C�����ͬ���ɷ�����֪��b��Һ�����Ի����ԣ���A���ȷ��D�����
6��[2010��ɽ�����ۣ�28]ʵ������Zn��ϡ������ȡH2����Ӧʱ��Һ��ˮ�ĵ���ƽ��___�ƶ�(����������������������������)�����������������Լ��е�____������H2�����ʽ�����
a��NaNO3�������� b��CuSO4 c��Na2SO4 d��NaHSO3
�������ҡ�b
��������Ӧ����������H����c(H��)��С��ˮ�ĵ���ƽ�������ƶ���
a��c�Է�Ӧ��Ӱ�죬b��Zn�û���Cu���γ�Cu��Znԭ��أ���Ӧ��������dʹ��Ӧ���ʱ�����
7��[2012���㽭���ۣ�26(3)]��֪��I2��2S2O===S4O��2I����ijѧϰС��������ӵ��������ⶨ����CuCl2��2H2O���������(��������I��������Ӧ������������)�Ĵ��ȣ��������£�ȡ0.36 g��������ˮ���������KI���壬��ַ�Ӧ�����ɰ�ɫ��������0.100 0 mol��L��1 Na2S2O3����Һ�ζ�������ζ��յ�ʱ������Na2S2O3����Һ20.00 mL��
����ѡ��________���ζ�ָʾ�����ζ��յ��������__________��
��CuCl2��Һ��KI��Ӧ�����ӷ���ʽΪ__________________��
����������CuCl2��2H2O�������ٷ���Ϊ__________��
������������Һ����ɫ��ȥ������һ��ʱ���ɫ
��2Cu2����4I��===2CuI����I2����95%
������������ӵ��������ⶨ����CuCl2��2H2O���������Ĵ��ȵĻ���ԭ����CuCl2����I������I2����Na2S2O3����Һ�ζ����ɵ�I2����������Һ��I2����ɫ���ʿ��õ�����Һ��ָʾ�����ﵽ�ζ��յ�ʱ����Һ����ɫ�����ɫ���Ұ��������Һ���ָ�ԭ������ɫ��
��CuCl2��KI����������ԭ��Ӧ�����ӷ���ʽΪ2Cu2����4I��===2CuI����I2��
���������Ϣ�ɵù�ϵʽ��2Cu2����I2��2S2O������n(CuCl2��2H2O)��n(Cu2��)��n(S2O)��0.100 0 mol��L��1��20.00��10��3 L��2.000��10��3 mol��m(CuCl2��2H2O)��2.000��10��3 mol��171 g��mol��1��0.342 g��������CuCl2��2H2O����������Ϊ��100%��95%��
8��[2009���㽭���ۣ�28(4)]���Ȼ���ֲ�Ʒ������õ��IJ������г�������Ԫ�أ�Ϊ�˷�������������Ԫ�صĺ������Ƚ�������Ԥ������ʹ��Ԫ�ػ�ԭ��Fe2�� ������KMnO4����Һ�����������½���������ԭ�ζ�����Ӧ�����ӷ���ʽ5Fe2����MnO��8H��==5Fe3����Mn2����4H2O
���ζ�ǰ�Ƿ�Ҫ�μ�ָʾ����________(����������������)����˵�����ɣ�__________��
��ijͬѧ��ȡ5.000 g�������Ԥ������������ƿ�����Ƴ�100 mL��Һ����ȡ25.00 mL������Һ����1.000��10��2 mol�� L��1 KMnO4����Һ�ζ����ﵽ�ζ��յ�ʱ�����ı���Һ20.00 mL�������������Ԫ�ص�����������________��
��������MnO��ɫ���ʲ�������ָʾ������4.48%
����������MnO��������ɫ���ʲ���������ָʾ����
���ɹ�ϵʽ
5Fe2��������MnO
5 1
n(Fe2��) 20.00��10��3 L��1.000��10��2 mol��L��1 �����25.00 mol������Һ��n(Fe2��)��0.001 mol�����Բ���������Ԫ�ص��������� w(Fe)����100%��4.48%
9��(2009���Ĵ����ۣ�26��)������������Ҫ������������ԭ��������ˮ��Һ�ֳ�Ϊ˫��ˮ��������������ɱ����Ư�ȡ�ij��ѧ��ȤС��ȡһ�����Ĺ���������Һ��ȷ�ⶨ�˹�������ĺ�������̽���˹�����������ʡ��ⶨ��������ĺ��� ������д���пհף�
(1)��ȡ10.00 mL�ܶ�Ϊ�� g��mL��1�Ĺ���������Һ��250 mL________(����������)�У���ˮϡ�����̶ȣ�ҡ�ȡ���ȡϡ�ͺ�Ĺ���������Һ25.00 mL����ƿ�У�����ϡ�����ữ��������ˮϡ�ͣ�������������
(2)�ø�����ر���Һ�ζ������������䷴Ӧ�����ӷ���ʽ���£��뽫������ʵĻ�ѧ����������ѧʽ��д�ڷ����
MnO��H2O2��H��===Mn2����H2O��
(3)�ζ�ʱ����������ر���Һע��______(������ʽ��������ʽ��)�ζ����С��ζ������յ��������_________________��
(4)�ظ��ζ����Σ�ƽ������c mol��L��1 KMnO4����ҺV mL����ԭ����������Һ�й����������������Ϊ_____________________��
(5)���ζ�ǰ�ζ��ܼ����������ݣ��ζ���������ʧ����ⶨ���________(����ƫ��������ƫ��������������)��
����(1)����ƿ
(2)2��5��6��2��8��5��O2
(3)��ʽ������һ�θ��������Һ����Һ��dz��ɫ����30���ڲ���ɫ
(4) (5)ƫ��
������(1)������ѡ�ø�������Ӧ��ѡ������ƿ��
(2)��ȱ����ʽ��ƽ����Ӧȷ��ȱʲô��������֪ȱ����O2�����ݵ���ת���غ㣬��ƽ��ѧ����ʽ��
(3)���ڸ�����ر���Һ����ǿ�����ԣ�����ֻ��ʹ����ʽ�ζ��ܡ��ζ������յ�������ǣ�����һ�θ��������Һ����Һ��dz��ɫ����30���ڲ���ɫ��
(4)������ƽ�Ļ�ѧ����ʽ�������������������������ԭ����������Һ�й����������������Ϊ��
(5)���ζ�ǰ�ζ��ܼ����������ݣ��ζ���������ʧ����һ������Һռ�������ݵ��������û�е�����ƿ����ⶨ���ƫ�ߡ�
���̺�ǡ�
����һ���к͵ζ�������ָʾ����ѡ��
1������֪Ũ�ȵ�NaOH��Һ�ⶨijH2SO4��Һ��Ũ�ȣ��ο���ͼ��ʾ���±���ѡ����ȷѡ�� (����)
|
ѡ�� |
��ƿ����Һ |
�ζ�������Һ |
ѡ��ָʾ�� |
ѡ�õζ��� |
|
A |
�� |
�� |
ʯ�� |
��ʽ�ζ��� |
|
B |
�� |
�� |
��̪ |
��ʽ�ζ��� |
|
C |
�� |
�� |
���� |
��ʽ�ζ��� |
|
D |
�� |
�� |
��̪ |
��ʽ�ζ��� |
�𰸡�D
�����������Ĺؼ��ǣ�����ȷ�ᡢ��ʽ�ζ���ʹ��ʱ��ע�������ָʾ���ı�ɫ��Χ����ʽ�ζ��ܲ���ʢ�ż����ʽ�ζ��ܲ���ʢ���ᣬָʾ��Ӧѡ����ɫ�仯���Եķ�̪����ȣ�����ѡ��ʯ����Ҫע��������к͵ζ��У������DZ���Һ�ζ�������Һ�����Ǵ�����Һ�ζ���Һ��ֻҪ������ȷ�����ܵõ���ȷ�Ľ����
2��ʵ��������3�����ָʾ������pH��ɫ��Χ���£�
���ȣ�3.1��4.4��ʯ�5.0��8.0����̪��8.2��10.0
��0.100 0 mol��L��1 NaOH��Һ�ζ�δ֪Ũ�ȵ�CH3COOH��Һ����Ӧǡ����ȫʱ��������������ȷ���� (����)
A����Һ�����ԣ���ѡ�ü��Ȼ��̪��ָʾ��
B����Һ�����ԣ�ֻ��ѡ��ʯ����ָʾ��
C����Һ�ʼ��ԣ���ѡ�ü��Ȼ��̪��ָʾ��
D����Һ�ʼ��ԣ�ֻ��ѡ�÷�̪��ָʾ��
�𰸡�D
������NaOH��Һ��CH3COOH��Һǡ�÷�Ӧ����CH3COONaʱ��CH3COO��ˮ���Լ��ԣ�����̪�ı�ɫ��ΧΪ8.2��10.0���ȽϽӽ�����˴�ΪD��
��������ᡢ���к͵ζ��������������ݴ���
3��ʵ��������һδ֪Ũ�ȵ�ϡ���ᣬijѧ����0.10 mol��L��1 NaOH����Һ���вⶨ�����Ũ�ȵ�ʵ�顣�����������գ�
ȡ20.00 mL�������������ƿ�У����μ�2��3�η�̪��ָʾ�������Լ����Ƶ�NaOH����Һ���еζ����ظ������ζ�����2��3�Σ���¼�������¡�
|
��� |
NaOHŨ��(mol��L��1) |
NaOH���(mL) |
������������(mL) |
|
1 |
0.10 |
22.62 |
20.00 |
|
2 |
0.10 |
22.72 |
20.00 |
|
3 |
0.10 |
22.80 |
20.00 |
(1)�ζ��ﵽ�յ�ı�־��_______________________��
(2)�����������ݣ��ɼ�����������Ũ��ԼΪ__________(������λ��Ч����)��
(3)��ȥ��ʽ�ζ��������ݵķ���Ӧ������ͼ��ʾ�����е�________��Ȼ�����ἷѹ������ʹ���첿�ֳ�����Һ��
![]()
(4)������ʵ���У����в���(����������ȷ)����ɲⶨ���ƫ�ߵ���________(����ĸ���)��
A���ζ��յ����ʱ����
B����ʽ�ζ���ʹ��ǰ��ˮϴ��δ�ô���������ϴ
C����ƿˮϴ��δ����
D������NaOH�������Na2CO3����
E����ʽ�ζ��ܼ��첿�������ݣ��ζ�����ʧ
�𰸡�(1)���һ��NaOH��Һ���룬��Һ����ɫǡ�ñ��dz��ɫ�Ұ�����ڲ���ɫ��(2)0.11 mol��L��1��(3)����(4)DE
����������ָʾ����������Һ�������Һ�е���ɫ�仯�����ǿ����ж��кͷ�Ӧ�Ƿ�ǡ�ý�����ȫ�����������Ũ��ʱ��Ӧ���������к͵ζ���ƽ��ֵ����NaOH��ҺŨ�ȼ�����Һ�����Ҳһ������ֻ��NaOH��Һ�����ƽ��ֵ���ɡ����ݼ�ʽ�ζ��ܵĹ����֪�������ܼ��ɽ����е������ų���
4��ijѧ������֪���ʵ���Ũ�ȵ��������ⶨδ֪���ʵ���Ũ�ȵ�NaOH��Һʱ��ѡ�������ָʾ��������д���пհף�
(1)�ñ�������ζ������NaOH��Һʱ����������ʽ�ζ��ܵĻ���������ҡ����ƿ���۾�ע��________��ֱ�������һ���������Һ�ɻ�ɫ��Ϊ��ɫ����______Ϊֹ��
(2)���в����п���ʹ����NaOH��Һ��Ũ����ֵƫ�͵���________��
 A����ʽ�ζ���δ�ñ�������ϴ��ֱ��ע�������
A����ʽ�ζ���δ�ñ�������ϴ��ֱ��ע�������
B���ζ�ǰʢ��NaOH��Һ����ƿ������ˮϴ����û�и���
C����ʽ�ζ����ڵζ�ǰ�����ݣ��ζ���������ʧ
D����ȡ�������ʱ����ʼ���Ӷ������ζ�����ʱ���Ӷ���
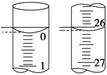
(3)���ζ���ʼ�ͽ���ʱ����ʽ�ζ����е�Һ����ͼ��ʾ������ʼ����Ϊ________mL���յ����Ϊ________mL������������Һ�����Ϊ________mL��
(4)ijѧ������3��ʵ��ֱ��¼�й��������±���
|
����� |
����NaOH��Һ�����/mL |
0.100 0 mol��L��1��������/mL |
||
|
�ζ�ǰ�̶� |
�ζ���̶� |
��Һ���/mL |
||
|
��һ�� |
25.00 |
0.00 |
26.11 |
26.11 |
|
�ڶ��� |
25.00 |
1.56 |
30.30 |
28.74 |
|
������ |
25.00 |
0.22 |
26.31 |
26.09 |
�����ϱ�������ʽ�����NaOH��Һ�����ʵ���Ũ�ȡ�
�𰸡�(1)��ƿ����Һ��ɫ�仯���ڰ�����ڲ���ɫ��(2)D��(3)0.00��26.10��26.10
(4)����26.10 mL��c(NaOH)����0.104 4 mol��L��1
������ѵ����
1��Ī������һ�ֳ����ζ�������K2CrO4Ϊָʾ�����ñ���������Һ�ζ�����Һ�����вⶨ��Һ��Cl����Ũ�ȡ���֪��
|
���� ���� |
AgCl |
AgBr |
AgCN |
Ag2CrO4 |
AgSCN |
|
��ɫ |
�� |
dz�� |
�� |
ש�� |
�� |
|
�ܽ��(mol��L��1) |
1.34��10��6 |
7.1��10��7 |
1.1��10��8 |
6.5��10��5 |
1.0��10��6 |
(1)�ζ��յ��������__________��
(2)����AgNO3��Һ�ζ�NaSCN��Һ����ѡΪ�ζ�ָʾ������_______��
A��NaCl B��BaBr2 C��Na2CrO4
�պôﵽ�ζ��յ�ʱ�����������ӷ�Ӧ����ʽΪ___________��
����(1)�������һ�α���Һ������ש��ɫ����
(2)C��2Ag����CrO===Ag2CrO4��
������(1)���ݳ����ζ�����ԭ������֪��Һ��Ag����Cl���ȷ�Ӧ��Cl����������ٺ�ָʾ����Ӧ����Ag2CrO4ש��ɫ�������ɴ˿�֪�ζ��յ�ʱ����ɫ�仯��
(2)����AgNO3��Һ�ζ�NaSCN��Һʱ����ѡ���ָʾ����Ag����Ӧ�����ɳ������ܽ��Ӧ����AgSCN���ܽ�ȣ���������ݿ��Կ����ܽ�ȱ�AgSCN�����AgCl��Ag2CrO4����������AgCl�ǰ�ɫ����������Ӧѡ��Na2CrO4Ϊָʾ���������ڵζ��յ�ʱ��������ɫ�������Եı仯(��ɫ��ש��ɫ)��ָʾ�ζ��պôﵽ�յ㣬��ʱ�����ӷ�Ӧ����ʽΪ2Ag����CrO===Ag2CrO4����
2��KMnO4��Һ������������ԭ��Ӧ�ζ��ı�Һ������KMnO4��ǿ�����ԣ�������Һ�����ױ������л�ˮ�е�ijЩ������ԭ�����ʻ�ԭ����������������MnO(OH)2���������KMnO4����Һ�IJ���������ʾ��
����ȡ�Զ�����������KMnO4��������ˮ�У�����Һ���Ȳ�������1 h�������ײ���©�����˳�ȥ���ܵ�MnO(OH)2�������˵õ���KMnO4��Һ��������ɫ�Լ�ƿ�����ڰ�����������������ԭ�ζ���������70��80 ���������û��Լ�(���ȸߡ���Է��������ϴ��ȶ��ԽϺõ�����)��Һ�궨��Ũ�ȡ�
��ش��������⣺
(1)ȷ��ȡһ�������KMnO4��Һ��Ҫʹ�õ�������____________��
(2)�����������У����ڱ궨KMnO4��Һ�Ļ��Լ����ѡ��________(�����)��
A��H2C2O4��2H2O B��FeSO4
C��Ũ���� D��Na2SO3
(3)��ȷ��ȡW g��ѡ�Ļ��Լ�����ˮ���500 mL��Һ��ȡ25.00 mL������ƿ�У���KMnO4��Һ�ζ����յ㣬����KMnO4��ҺV mL��KMnO4��Һ�����ʵ���Ũ��Ϊ___mol��L��1��
(4)���÷������ܵ�KMnO4����Һȥ�ⶨˮ����Fe2���ĺ�������õ�Ũ��ֵ��__(����ƫ��������ƫ����������Ӱ����)��
����(1)��ʽ�ζ��ܡ�(2)A��(3)��(4)ƫ��
������(1)KMnO4��Һ����ǿ�����ԣ��ܽ���ʽ�ζ����¶˵��ܸ�ʴ�����Բ����ü�ʽ�ζ�����ȡ����������ʽ�ζ�����ȡ��
(2)H2C2O4��2H2O�ڳ��³�ѹ�����ȶ��Ľᾧˮ���
FeSO4�ڿ����в��ȶ��ױ���������Ԫ�صĻ��ϼ۴ӣ�2���ߵ���3��Ũ�����ӷ���Na2SO3�ڿ����в��ȶ��ױ�������Na2SO4��
(3)���ݵ�ʧ�����غ�ԭ���й�ϵʽ��5(H2C2O4��2H2O)��2KMnO4����KMnO4��Һ��Ũ��Ϊ
c(KMnO4)���� mol��L��1��
(4)�ڷ��ù����У����ڿ����л�ԭ�����ʵ����ã�ʹKMnO4��Һ��Ũ�ȱ�С�ˣ���ȥ�ζ�ˮ���е�Fe2��ʱ������KMnO4��Һ(����Һ)������������¼��������c(Fe2��)�����ⶨ�Ľ��ƫ�ߡ�
����ȴ�������
��һƪ����ʮһ��Ԫ ˮ��Һ�е�����ƽ�⣨2��
��һƪ����ʮһ��Ԫ ˮ��Һ�е�����ƽ�⣨4��
