高一化学必修2第一章单元检测
2015-10-16 09:52:03 来源: 撰稿:董啸 摄影摄像: ; 评论:0 点击:
高一化学必修2第一章单元检测
可能用到的相对原子质量: H-1 C-12 N-14 O-16 S-32 Cl-35.5 Na-23
第Ⅰ卷(选择题)
一、选择题(包括10小题,每小题2分,共20分。每小题只有一个选项符合题意)
1.据中央电视台11月15日焦点访谈报道2007年6月中旬,在黑龙江省哈尔滨市的一个居民小区,同住一栋楼的两家人相继得上一种怪病:红细胞、白细胞、血小板严重偏低。经黑龙江省辐射监督管理站的专家检测,发现是放射性物质铱-192在作怪。则![]() 的中子数和质子数之差为( )
的中子数和质子数之差为( )
A.115 B.38 C.269 D.154
2. 1869年,俄国化学家门捷列夫制作出了第一张元素周期表,提示了化学元素间的内在联系,成为化学史上的重要里程碑之一。下列有关元素周期表的说法正确的是( )
A.元素周期表有七个周期 B.元素周期表有18个族
C.IA族的元素全部是金属元素 D.短周期是指第一、二、三、四周期
3.核外电子层结构相同的一组微粒是( )
A.Mg2+、Al3+、Cl-、Ne B.Na+、F-、S2-、Ar
C.K+、Ca2+、S2-、Ar D.Mg2+、Na+、Cl-、S2-
4.下列分子中的电子数与HF含有的电子数相同,且只有两个极性共价键的是( )
A.CO2 B.H2O C.N2O D.CH4
5.下列说法中正确的是( )
A.同周期元素的电子层数都相同 B.同族元素的最外层电子数一定相同
C.最外层电子数相同的元素都在同一族
D.周期表是按相对原子质量逐渐增大的顺序从左到右排列的
6.下列物质中属于共价化合物的是( )
A.Na2O2 B.I2 C.NaHSO4 D.HNO3
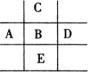 7.右图为周期表的一部分,已知A、B、C、D、E五种元素原子核外共有
7.右图为周期表的一部分,已知A、B、C、D、E五种元素原子核外共有
85个电子,E原子核外共有四个电子层,B元素是( )
A.P B.Mg C.Cl D.Si
8. 随着卤素原子半径的增大,下列递变规律正确的是 ( )
A.单质熔、沸点逐渐降低 B.气态氢化物稳定性逐渐增强
C.卤素离子的还原性逐渐增强 D.单质的氧化性逐渐增强
9.第四周期某主族元素的原子最外层有两个电子,下列关于此元素的叙述正确的是( )
A.原子半径比钾的原子半径大 B.氯化物难溶于水
C.其氢氧化物的碱性比NaOH强 D.碳酸盐难溶于水
10.无机化学命名委员会在1989年作出决定,把长式元素周期表原先的主、副族及族号取消,由左到右改为18列。按此规定,下列说法中错误的是 ( )
A.第15列元素的最高价氧化物的化学式是R2O3
B.第1列和第17列元素单质熔、沸点变化趋势相反
C.第11列中肯定没有非金属元素
D.在18列元素中,第3列的元素种类最多
11.具有下列价电子数的原子,最难形成离子的是
A.L层6个 B.L层4个 C.M层2个 D.L层7个
12.某元素最高正价与负价绝对值之差为4,该元素的离子跟与其核外电子排布相同的离子形成的化合物是( )
A.Na2S B.MgS C.MgO D.NaF
13.医疗上常用含131I-的药物进行甲状腺疾病的诊断。已知碘元素的核电荷数为53,则下列关于131I-的说法中正确的是 ( )
A. 131I-的质量数是132 B.131I-的核外有54个电子
C. 131I-的核内有53个中子 D.131I-的核内有74个质子
14.下列物质中,既有离子键,又有共价键的是( )
A.CaCl2 B.HNO3 C.H2O D.NH4F
15.有![]() 和
和![]() 两离子,它们具有相同的电子层结构,则a和m、n、b的关系为( )
两离子,它们具有相同的电子层结构,则a和m、n、b的关系为( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
16.下列说法中不正确的是( )
A.在共价化合物中也可能含有离子键
B.非金属单质分子中的化学键一定是共价键
C.含有共价键的化合物不一定是共价化合物
D.含有离子键的化合物一定是离子化合物
17.下列各组大小顺序不正确的是 ( )
A.粒子半径:S2- > Cl-> Na+ > Mg2+ B.热稳定性:SiH4 < PH4 < H2S < HCl
C.酸性:H3PO4 > H2SO4 > HClO4 D.还原性:HF < HCl < HBr < HI
18.已知X、Y、Z三种元素的最高价氧化物对应的水化物的酸性由强到弱的顺序:HZO4>H2YO4> H3XO4 ,下列判断正确的是 ( )
A.3种元素阴离子还原性按X、Y、Z的顺序增强
B.单质的氧化性按X、Y、Z的顺序减弱
C.气态氢化物的稳定性按X、Y、Z的顺序减弱
D.原子半径按X、Y、Z的顺序减小
19.下列有关碱金属铷(Rb)的叙述中,正确的是 ( )
A.铷金属性比钠弱 B.硝酸铷是离子化合物,易溶于水
C.氢氧化铷是弱碱 D.在钠、钾、铷三种单质中,铷的熔点最高
20.第七周期为不完全周期,若将来的发展把这一周期元素全部排满。则下列关于第七周期元素的推论可能错误的是 ( )
A.第七周期排满时有32种元素
B.第七周期排满时最后一种单质在常温下不易发生化学反应
C.第七周期第ⅦA族元素原子序数117,是一种金属元素
D.第七周期第ⅢA族元素的氢氧化物与Al(OH)3具有相似的化学性质
21.对于IVA族元素,下列叙述中不正确的是B
A.SiO2和CO2中,Si和O,C和O之间都是共价键
B.C、Si和Ge的最外层电子数都是4,次外层电子数都是8
C.CO2 和 SiO2 都是酸性氧化物,在一定条件下都能和氧化钙反应
D.该族元素的主要化合价式-4和+2
22.下列说法正确的是C
A.SiH4比CH4稳定 B.Na和Cs属于第族元素,Cs失电子能力比Na的强
C.O2-半径比F-的小 D.P和As属于第族元素,H3PO4酸性比H3AsO4的弱
23.元素X、Y和Z可结合形成化合物XYZ3;X、Y和Z的原子序数之和为26;Y和Z在同一周期。下列有关推测正确的是B
A.XYZ3是一种可溶于水的酸,且X与Y可形成共价化合物XY
B.XYZ3是一种微溶于水的盐,且X与Z可形成离子化合物XZ
C.XYZ3是一种易溶于水的盐,且Y与Z可形成离子化合物YZ
D.XYZ3是一种离子化合物,且Y与Z可形成离子化合物YZ3
24.有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是A
A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
D.若Y的最高正价为+ m,则X的最高正价一定为+ m
25.下列叙述正确的是 ( )
A.金刚石和石墨的性质相同 B.40K和 40Ca原子中质子数和中子数都不相等
C.H2和D2互为同位素 D.某物质只含一种元素,该物质一定是纯净物
26.下列表示电子式的形成过程正确的是( )
A.![]() B.
B. ![]()
C.![]() D.
D.![]()
27.下列叙述中能肯定金属A比金属B活泼的是( )
A.A原子的最外层电子数比B原子的最外层电子数少
B.A原子的电子层数比B原子的电子层数多
C.1 mol A从酸中置换出的H2比1 mol B从酸中置换出的H2多
D.常温时,A能从水中置换出氢气,而B不能
28.两种元素原子的核外电子层数之比与最外层电子数之比相等,则在周期表的前10号元素中,满足上述关系的元素共有 ( )
A.1对 B.2对 C.3对 D.4对
第Ⅱ卷(非选择题)
二、填空题(共22分)
29.(8分)写出下列微粒的符号及结构示意图
①原子核内有10个质子的原子_______ _
②核外有10个电子的二价阳离子_____ ___
③核外有18个电子的一价阴离子___ _____
④L为最外层,L层电子数是K层电子数的3倍的原子____ ____
30.(14分)A、B、C、D、E为元素周期表中前三周期的主族元素,它们的原子序数按A、B、C、D、E的顺序增大。A的最外层电子数是次外层电子数的2倍,C与E最外层电子数相等,E的最高价氧化物中含氧60%,D与C可形成D2C、D2C2两种离子化合物。填写下列空白:
(1)写出上述五种元素的元素符号:A_____,B_____,C_____,D_____,E_____。
(2)写出D2C2的电子式______________。
(3)用电子式表示AC2化合物的形成过程_______________________________________
三、推断题(28分)
31.(14分)有A、B、C、D、E五种元素,元素A的一种原子无中子,元素B和C都有2个电子层,它们能生成无色无嗅的气体BC2,元素D有三个电子层,它和元素C属于同一主族,D和C生成有刺激性气味的气体DC2;元素E的阳离子E+的电子层结构与Ar的电子层结构相同,试回答:
(1)它们的元素符号是:A________B________C________D________E________。
(2)A与B形成的化合物以________键结合, C和E的化合物以________键结合。
32.(14分)已知A、B、C、D 4种元素,都是位于元素周期表中第一、二周期的元素,原子序数按A、C、D、B的顺序递增,A与C最外层电子数相同且都是1,B与C具有相同的电子层数,它们的最外层电子数相差6个.D元素最外层电子数是次外层电子数的3倍,试回答:
(1)A、B、C、D的元素名称及元素在周期表中的位置.
(2)A与B、C与D都以何种化学键结合?形成什么型的化合物?分别写出它们的电子式.
30.a、b、c、d、e是短周期元素,周期表中a与b、b与c相邻;a与e的最外层电子数之比为2:3,b的最外层电子数比e的最外层电子数少1个;常见化合物d2c2与水反应生成c的单质,且溶液使酚酞试液变红。
(1)e的元素符号是__________。
(2)a、b、c的氢化物稳定性顺序为(用分子式表示)__________________;b的氢化物和b的最高价氧化物的水化物反应生成Z,则Z中的化学键类型为__________________;ab-离子的电子式为____________。
(3)由a、c、d形成化合物的水溶液显碱性,其原因是(用离子方程式表示)_______________。
(4)一定量的d2c2与ac2反应后的固体物质,恰好与0.8 mol稀盐酸溶液完全反应,并收集到0.25 mol气体,则用物质的量表示该固体物质的组成为__________________、___________________。
33.由某碱金属(R)及其氧化物(R2O)组成的混合物8.1 g,与水充分反应后,经蒸发、结晶,得到干燥的固体12 g,试通过计算确定该碱金属的名称以及混合物的组成。
上一篇:无机化学部分
下一篇:高 一 化 学 试 题
